题目内容
常温下,用0.1000 mol·L-1 NaOH溶液分别滴定20.00 mL 0.1000 mol·L-1盐酸和20.00 mL 0.1000 mol·L-1醋酸溶液,得到两条滴定曲线,如下图所示,若以HA表示酸,下列说法正确的是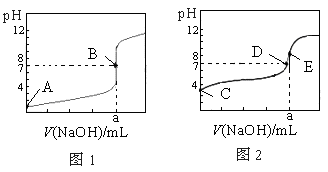
A.滴定盐酸的曲线是图2
B.达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl)
C.达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A-)
D.当0 mL<V(NaOH)<20.00 mL时,对应混合液中各离子浓度大小顺序为c(A-)>c(Na+)>c(H+)>c(OH-)
C
解析试题分析:A、滴定开始时0.1000mol/L盐酸pH=1,而0.1000mol/L醋酸pH>1,所以滴定盐酸的曲线是图1,故A不正确;B、达到B、E状态时,消耗的氢氧化钠物质的量是相等的,根据反应原理:HCl~NaOH,CH3COOH~NaOH,反应消耗的n(CH3COOH)=n(HCl),故B错误;C、达到B、D状态时,溶液是中性的,此时c(H+)=c(OH-),根据电荷守恒:c(Na+)+c(H+)=c(A-)+c(OH-),则两溶液中离子浓度均为 c(Na+)=c(A-),故C正确;D、当0 mL<V(NaOH)<20.00 mL时,酸相对于碱来说是过量的,所得溶液是生成的盐和酸的混合物,假设当加入的氢氧化钠极少量时,生成了极少量的钠盐(氯化钠或是醋酸钠),剩余大量的酸,此时c(A-)>c(H+)>c(Na+)>c(OH-),故D错误,答案选C。
考点:考查NaOH与强酸、弱酸的反应,涉及盐类的水解和溶液离子浓度的大小比较知识

下列说法正确的是
| A.向AgCl悬浊液中加入少量NaCl固体后振荡,c(Cl-)增大,KsP (AgCl)增大 |
B.某溶液中由水电离出的 时,则该溶液的pH一定为14-a 时,则该溶液的pH一定为14-a |
| C.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后溶液的pH等于7,则混合溶液 中: 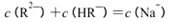 |
D.相同物质的量浓度的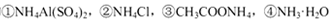 溶液中,c (NH4+)由大到小的顺序是:①>②>③>④ 溶液中,c (NH4+)由大到小的顺序是:①>②>③>④ |
室温下,将一元酸HA溶液和NaOH溶液等体积混合,实验数据如表:
| 实验编号 | 起始浓度c(HA) | 起始浓度c(NaOH) | 反应后溶液的pH |
| ① | 0.1 mol·L-1 | 0.1 mol·L-1 | 9 |
| ② | x | 0.2mol·L-1 | 7 |
下列说法正确的是
A.实验①反应前HA溶液中c(H+)=c(OH-)+ c(A-)
B.实验①反应后溶液中c(A-)>c(Na +)
C.实验②反应前HA溶液浓度x>0.2 mol·L-1
D.实验②反应后溶液中c(A-)+ c(HA)= c(Na+)
已知常温下BaSO4的溶解度为2.33×10-4g,类似于水的离子积,难溶盐AmBn也有离子积Ksp且Ksp=〔C(An+)〕m·〔C(Bm-)〕n,,则BaSO4的Ksp约为
| A.2.33×10-4 | B.1×10-5 | C.1×10-10 | D.1×10-12 |
250C时,pH=3的HNO3,下列该硝酸说法正确的是
| A.该硝酸中水电离出的c(H+)=1.0×10-3mol/L |
| B.加水稀释到原溶液体积的100倍,硝酸溶液的pH为5 |
| C.相同温度下,pH=3的CH3COOH溶液的物质的量浓度与该硝酸相同 |
| D.该硝酸中加入少量的Zn粒产生H2 |
对滴有酚酞试液的下列溶液,操作后颜色变深的是
| A.明矾溶液加热 | B.CH3COONa溶液加热 |
| C.氨水中加入少量NH4Cl | D.小苏打溶液中加入少量的NaCl固体 |
室温下,将1.000 mol·L-1盐酸滴入20.00 mL1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是( )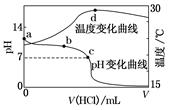
| A.a点由水电离出的c(H+)=1.0×10-14 mol·L-1 |
| B.b点:c(NH4+)+c(NH3·H2O)=c(Cl-) |
| C.c点:c(Cl-)=c(NH4+) |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |