下列叙述正确的是
| A.FeCl3溶液中加入镁粉有气泡产生 |
| B.C12、SO2均能使品红溶液褪色,说明二者均有漂白性 |
| C.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| D.向饱和NaC1溶液中先通入足量CO2,再通入足量NH3,可析出NaHCO3晶体 |
在25℃时,向50.00 mL未知浓度的CH3COOH溶液中逐滴加入0.5 mol·L-1的NaOH溶液。滴定过程中,溶液的pH与滴入NaOH溶液体积的关系如图所示,则下列说法中,正确的是
| A.该中和滴定过程,最宜用石蕊作指示剂 |
B.图中点②所示溶液中, |
| C.图中点①所示溶液中水的电离程度大于点③所示溶液中水的电离程度 |
D.滴定过程中的某点,会有 的关系存在 的关系存在 |
100℃时,下列各溶液中,离子的物质的量浓度关系正确的是:
| A.pH=11的氨水中:c(OH-)=3.0mol·L-1 |
| B.呈中性的醋酸和醋酸钠的混合溶液中:c(Na+)=c(CH3COO-) |
| C.pH=2的稀盐酸中,c(H+)=c(Cl-) |
| D.pH=8的Na2SO3溶液中,c(Na+)>c(SO32-)>c(HSO3-)>c(OH-) |
今有室温下四种溶液,有关叙述正确的是
| | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
B.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
C.①、④两溶液等体积混合,所得溶液中c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.VaL④与VbL②溶液混合后,若混合后溶液pH=4,则Va∶Vb= 9∶11
HF为一元弱酸,在0.1mol·L-1 NaF溶液中,离子浓度关系正确的是
| A.c(Na+)>c(F-)>c(H+)>c(OH-) | B.c(Na+)>c(OH-)>c(F-)>c(H+) |
| C.c(Na+) + c(OH-)=c(F-) + c(H+) | D.c(Na+) + c(H+)=c(F-) + c(OH-) |
已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.2mol·L-1HF溶液中加入1 L 0.2 mol·L-1CaCl2溶液,则下列说法中,正确的是( )
| A.25℃时,0.1 mol·L-1HF溶液中pH=1 | B.Ksp(CaF2)随温度和浓度的变化而变化 |
| C.该体系中有CaF2沉淀产生 | D.加入CaCl2溶液后体系中的c(H+)浓度不变 |
下列说法正确的是
| A.在CuSO4溶液中加入PbS,可转变为铜蓝(CuS),则Ksp(PbS)<Ksp(CuS) |
| B.在NaHS溶液中,加入少量CuCl2粉末产生黑色沉淀,则pH增大 |
| C.加热条件下并加入大量水促进TiCl4水解,以制备TiO2固体 |
| D.铜制器皿放置过程中会生成铜绿是因为发生了析氢腐蚀 |
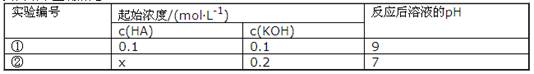
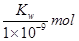 ·L-1
·L-1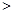 0.1mol·L-l
0.1mol·L-l