一定温度下,在体积一定的密闭容器中进行的可逆反应:C(s) + CO2(g)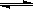 2CO(g),不能判断反应已经达到化学平衡状态的是
2CO(g),不能判断反应已经达到化学平衡状态的是
| A.v(CO2)= v(CO) | B.容器中总压强不变 |
| C.容器中混合气体的密度不变 | D.容器中CO的体积分数不变 |
对于达到化学平衡状态的可逆反应:N2 + 3H2 2NH3 + Q,下列叙述中正确的
2NH3 + Q,下列叙述中正确的
| A.反应物和生成物的浓度相等 | B.反应物和生成物的浓度不再变化 |
| C.降低温度,平衡混合物中NH3的浓度减小 | D.增大压强,不利于氨的合成 |
工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol 在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol 在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:
| 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4) | 0.50 | 0.30 | 0.18 | …… | 0.15 |
A.10 min内,T1时CH4的化学反应速率比T2时小 B.温度:T1<T2
C.ΔH:a < 0 D.平衡常数:K(T1)<K(T2)
在一密闭容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器容积增加一倍,达到新平衡时,B的浓度是原来的60%。则下列叙述正确的是( )
bB(g)达平衡后,保持温度不变,将容器容积增加一倍,达到新平衡时,B的浓度是原来的60%。则下列叙述正确的是( )
| A.a>b | B.平衡向正反应方向移动 |
| C.A的转化率减小 | D.B的质量分数减小 |
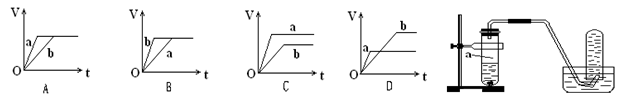
已知反应3A(g)+B(g)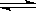 C(s)+4D(g) ΔH<0,下图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是( )
C(s)+4D(g) ΔH<0,下图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是( )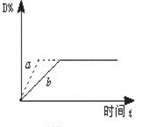
①增大B的浓度 ②升高反应温度
③缩小反应容器的体积(加压) ④加入催化剂
| A.①② | B.①③ | C.②③ | D.③④ |
下列条件下化学反应速率最大的是( )
| A.20℃0.1mol·L-1的盐酸溶液20 mL与0.5 g块状碳酸钙反应 |
| B.10℃ 0.1mol·L-1的盐酸溶液20 mL与1 g块状碳酸钙反应 |
| C.10℃ 0.2mol·L-1的盐酸溶液10mL与0.5g粉状碳酸钙反应 |
| D.20℃ 0.2mol·L-1的盐酸溶液10mL与0.5g粉状碳酸钙反应 |
反应H2(g)+ I2(g) 
 2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是( )
2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是( )
①单位时间内断裂n mol H-H键的同时形成2n mol H-I键 ②单位时间内生成n molI2的同时生成2n molHI
| A.②④⑤⑥ | B.②③④⑤ | C.①③④⑤ | D.全部 |