题目内容
反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在 5L密闭容器中进行,30秒后,NO的物质的量增加了0.3 mol,则此反应的平均速率v(x)(表示反应物的消耗速率或生成物的生成速率)为
A.v (O2)=" 0.0l" mol·L-1·s-1 B.v (NO)="0.002" mol·L-1·min-1
C.v (H2O)="0.003" mol·L-1·s-1 Dv (NH3)="0.001" mol·L-1·s-1
C
解析试题分析:根据v=△n/△tV代入数据计算得v(NO)v(NO)="0.002" mol·L-1·s-1,不同物质表示的速率之比等于其化学计量数之比,A、v(O2)="0.0025" mol·L-1·s-1,错误;B、v(NO)="0.002" mol·L-1·s-1,选项中单位错误,错误;C、v(H2O)="0.003" mol·L-1·s-1,正确;D、v(NH3)=v(NO)="0.002" mol·L-1·s-1,错误。
考点:考查化学反应速率的有关计算。

在一定温度下,反应:2A(s)+2B(g)  C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是
| A.单位时间内生成2a mol B,同时生成a molD |
| B.C的质量不再改变 |
| C.容器内的压强不随时间而变化 |
| D.混合气体的密度不再随时间而变化 |
25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:
Sn(s)+Pb2+(aq) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )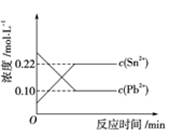
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0 |
| D.25 ℃时,该反应的平衡常数K=2.2 |
在一密闭容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器容积增加一倍,达到新平衡时,B的浓度是原来的60%。则下列叙述正确的是( )
bB(g)达平衡后,保持温度不变,将容器容积增加一倍,达到新平衡时,B的浓度是原来的60%。则下列叙述正确的是( )
| A.a>b | B.平衡向正反应方向移动 |
| C.A的转化率减小 | D.B的质量分数减小 |
T℃时在2L的密闭容器中X(g)与Y (g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图l所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论正确的是
A.容器中发生的反应可表示为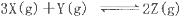 |
B.反应进行的前3 min内,用X表示的反应速率 |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
下列实验过程中曲线变化不正确的是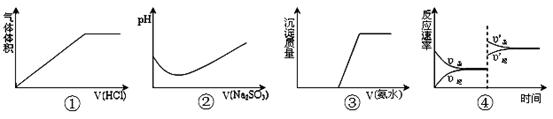
| A.①表示Na2CO3溶液中滴入稀盐酸 |
| B.②表示溴水中滴入Na2SO3溶液 |
| C.③表示HCl和MgCl2溶液中滴入氨水 |
D.④表示一定条件下反应:2SO2+O2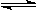 2SO3 ΔH< 0 ,达平衡后,增大压强 2SO3 ΔH< 0 ,达平衡后,增大压强 |
 C+5D反应中,表示该反应速率最快的是( )
C+5D反应中,表示该反应速率最快的是( ) 2B(g)+C(g)ΔH<0,在未用催化剂的条件下已达平衡,现要使正反应速率降低,c(B)减小,应采取的措施是
2B(g)+C(g)ΔH<0,在未用催化剂的条件下已达平衡,现要使正反应速率降低,c(B)减小,应采取的措施是 2SO3(g)在一个体积不变的密闭容器中反应,达到平衡状态的标志是( )
2SO3(g)在一个体积不变的密闭容器中反应,达到平衡状态的标志是( )