题目内容
对于达到化学平衡状态的可逆反应:N2 + 3H2 2NH3 + Q,下列叙述中正确的
2NH3 + Q,下列叙述中正确的
| A.反应物和生成物的浓度相等 | B.反应物和生成物的浓度不再变化 |
| C.降低温度,平衡混合物中NH3的浓度减小 | D.增大压强,不利于氨的合成 |
B
解析试题分析:达到化学平衡状态时反应物和生成物的浓度不再变化,并不一定是反应物和生成物的浓度相等,A错,B正确;反应放热,降低温度,平衡向正向移动,混合物中NH3的浓度最大,C错;增大压强,平衡向正向移动,有利于氨的合成,D错。
考点:化学平衡状态判断与平衡移动。

练习册系列答案
相关题目
对于可逆反应N2(g)+3H2(g)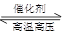 2NH3(g),在不同条件下的化学反应速率如下,其中表示反应速率最快的是
2NH3(g),在不同条件下的化学反应速率如下,其中表示反应速率最快的是
| A.υ(H2)=0.3mol/(L·min) | B.υ(N2)=0.2mol/(L·min) |
| C.υ(NH3)=0.25mol/(L·min) | D.υ(H2)=0.4mol/(L·min) |
下列关于化学反应的速率和限度的说法不正确的是( )
| A.任何可逆反应都有一定的限度 |
| B.影响化学反应速率的条件有温度、催化剂、浓度等 |
| C.化学平衡状态指的是反应物和生成物浓度相等时的状态 |
| D.决定反应速率的主要因素是反应物的性质 |
已知反应3A(g)+B(g)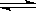 C(s)+4D(g) ΔH<0,下图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是( )
C(s)+4D(g) ΔH<0,下图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是( )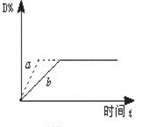
①增大B的浓度 ②升高反应温度
③缩小反应容器的体积(加压) ④加入催化剂
| A.①② | B.①③ | C.②③ | D.③④ |
在恒容密闭容器中,由CO合成甲醇:CO(g) + 2H2(g)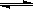 CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如右图所示,下列说法正确的是
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如右图所示,下列说法正确的是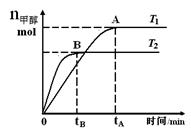
A.平衡常数K = 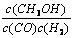 |
| B.该反应在T1时的平衡常数比T2时的小 |
| C.任意时刻,T2温度下的反应速率均大于T1温度下的速率 |
D.处于A点的反应体系从T1变到T2,达到平衡时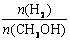 增大 增大 |
下列叙述不正确的是
| A.铁生锈、白磷燃烧均为自发放热过程 |
| B.冰融化过程其熵值增大 |
| C.高温高压下可以使石墨转化为金刚石是自发的化学反应 |
| D.同一物质固态时熵值最小 |
化学平衡状态I、II、III的相关数据如下表:
| 编号 | 化学方程式 | 平衡常数 | 温度 | |
| 979K | 1173K | |||
| I | Fe(s)+CO2(g) 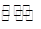 2 FeO(s)+CO(g) 2 FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| II | CO(g)+H2O(g) 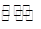 CO2(g)+H2(g) CO2(g)+H2(g) | K2 | 1.62 | b |
| III | Fe(s)+H2O(g)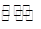 FeO(s)+H2(g) FeO(s)+H2(g) | K3 | a | 1.68 |
A.a>b B.增大压强,平衡状态II不移动
C.升高温度平衡状态III向正反应方向移动 D.反应II、III均为放热反应
100mL 6mol/L H2SO4跟过量锌粉反应,在一定温度,为了“减缓反应进行的速率,但又不影响生成H2的总量”,可向反应物中加入适量的 ( )
| A.Na2CO3溶液 | B.Na2CO3固体 | C.水 | D.NaNO3固体 |
 2C(气)达到平衡的标志是( )
2C(气)达到平衡的标志是( )