1919年,Langmuir提出等电子体的概念,由短周期元素组成的粒子,只要其原子数相同,各原子的最外层电子数之和相同,也可互称为等电子体。等电子体的结构相似、物理性质相似。根据上述原理,下列各对粒子中,空间结构相似的是
| A.SO2与O3 | B.CO2与NO2 | C.CS2与NO2 | D.PCl3与BF3 |
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的气态N4分子,其分子结构如右图所示。已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N N放出942 kJ热量,根据以上信息和数据,判断下列说法正确的是
N放出942 kJ热量,根据以上信息和数据,判断下列说法正确的是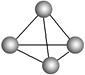
| A.N4属于一种新型的化合物 |
| B.N4分子中存在非极性键 |
| C.N4分子中N—N键角为109°28′ |
| D.1 mol N4转变成N2将吸收882 kJ热量 |
氯化钠是日常生活中人们常用的调味品,下列性质可以证明氯化钠中一定存在离子键的是
| A.具有较高的熔点 | B.熔融状态下能导电 |
| C.水溶液能导电 | D.常温下能溶于水 |
科学家在《Science》上发表论文,宣布发现了铝的超原子结构Al13和Al14,当这类超原子具有40个价电子(对于主族元素的原子,外围电子又称为价电子)时最稳定,在质谱仪上可检测到稳定到Al13-和Al142+。下列说法错误的是
| A.Al13和Al14互为同位素 |
| B.Al13超原子中Al原子间是通过共价键结合的 |
| C.Al13和Al的化学性质相似,都具有较强的还原性 |
| D.Al14和稀盐酸反应的化学方程式可表示为Al14+2HCl→Al14Cl2+H2↑ |
氯磺酸(HSO3C1)是一种易与水反应的强酸,可以在常温下用HCl+SO3→HSO3Cl制得,下列说法正确的是
| A.HSO3Cl具有强腐蚀性 |
| B.HSO3Cl也可以用浓盐酸与浓硫酸反应制得 |
| C.HSO3Cl与NaOH溶液反应生成产物只有NaSO3Cl |
| D.常温下,0.1mol的HSO3Cl溶于水制得1L溶液,pH等于1 |
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物Al2H6的球棍模型如下图所示,它的熔点为150℃,燃烧热极高。下列说法肯定错误的是
| A.Al2H6在固态时所形成的晶体是分子晶体 |
| B.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| C.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| D.氢铝化合物中可能存在组成为的物质(n为正整数) |
下列分子中,属于含有极性键的非极性分子的是
| A.PCl3 | B.H2S | C.P4 | D.C2H4 |
下列说法不正确的是
①非金属元素构成的单质中一定存在共价键;②非金属之间形成的化合物一定是共价化合物;③非金属的气态氢化物中一定存在极性共价键;④离子化合物中一定含有离子键;⑤金属元素和非金属元素形成的化合物一定是离子化合物;⑥在一种化合物中只能存在一种类型的化学键;⑦含共价键的化合物不一定是共价化合物;⑧含离子键的化合物一定是离子化合物;⑨氯化钠和HCl溶于水都发生电离,克服粒子间作用力的类型相同
| A.③④⑦⑧ | B.①③④⑦⑧ | C.①②⑤⑥⑨ | D.①④⑦⑨ |
下列说法不正确的是
①非金属元素构成的单质中一定存在共价键;②非金属之间形成的化合物一定是共价化合物;③非金属的气态氢化物中一定存在极性共价键;④离子化合物中一定含有离子键;⑤金属元素和非金属元素形成的化合物一定是离子化合物;⑥在一种化合物中只能存在一种类型的化学键;⑦含共价键的化合物不一定是共价化合物;⑧含离子键的化合物一定是离子化合物;⑨氯化钠和HCl溶于水都发生电离,克服粒子间作用力的类型相同
| A.③④⑦⑧ | B.①③④⑦⑧ | C.①②⑤⑥⑨ | D.①④⑦⑨ |