题目内容
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的气态N4分子,其分子结构如右图所示。已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N N放出942 kJ热量,根据以上信息和数据,判断下列说法正确的是
N放出942 kJ热量,根据以上信息和数据,判断下列说法正确的是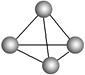
| A.N4属于一种新型的化合物 |
| B.N4分子中存在非极性键 |
| C.N4分子中N—N键角为109°28′ |
| D.1 mol N4转变成N2将吸收882 kJ热量 |
B
解析试题分析:A、N4是由氮元素形成的一种单质,不属于一种新型的化合物,A不正确;B、氮元素是活泼的非金属,氮元素与氮元素之间形成的是非极性键,B正确;C、N4是正四面体型结构,键角是60°,C不正确;D、已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N N放出942 kJ热量,则1 mol N4转变成N2时的反应热△H=6×167 kJ/mol-2×942 kJ/mol=-882 kJ/mol,即该反应是放热反应,因此1 mol N4转变成N2将放出882 kJ热量,D不正确,答案选B。
N放出942 kJ热量,则1 mol N4转变成N2时的反应热△H=6×167 kJ/mol-2×942 kJ/mol=-882 kJ/mol,即该反应是放热反应,因此1 mol N4转变成N2将放出882 kJ热量,D不正确,答案选B。
考点:考查分子结构、化合物与单质、化学键以及反应热的有关判断和计算

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
下列物质中,既含离子键又含共价键的是
| A.CaCl2 | B.NH4Cl | C.CCl4 | D.CO2 |
以下物质的分子可用比例模型 表示的是
表示的是
| A.CO2 | B.H2O | C.N2O | D.HClO |
下列分子中,属于含有极性键的非极性分子的是
| A.PCl3 | B.H2S | C.P4 | D.C2H4 |
把铜粉放入装有浓氨水的试管中,塞紧试管塞,振荡后发现试管塞越来越紧,且溶液逐渐变为浅黄色(近乎无色)溶液,打开试管塞后,溶液迅速变为蓝色溶液。则下列说法正确的是( )
| A.试管塞越来越紧,是因为反应消耗了大量NH3 |
| B.溶液逐渐变为浅黄色,是因为反应生成了少量的NO2 |
C.溶液迅速变为蓝色溶液,是因为反应生成了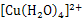 |
| D.上述反应原理可用于测定O2的含量 |
下列说法不正确的是
| A.HCl、HBr、HI的熔点沸点升高与范德华力大小有关 |
| B.H2O的熔点沸点大于H2S的是由于H2O分子之间存在氢键 |
| C.乙醇与水互溶可以用相似相溶原理解释 |
| D.甲烷与水分子间不能形成氢键这种化学 |
三氟化硼(BF3)是一种无色气体,用于制造火箭的高能燃料。已知BF3是非极性分子,下列描述正确的是
| A.BF3分子呈三角锥形 | B.BF3沸点低于BCl3 |
| C.B-F键键能低于B-Cl键 | D.F-B-F间的夹角为109°28′ |
下列分子中既有极性键,又有非极性键的是
| A.C2H4 | B.H2 | C.Na2O | D.NH3 |
下列说法正确的是( )
| A.离子键就是阴阳离子间的静电引力 |
| B.所有金属元素与所有非金属元素间都能形成离子键 |
| C.钠原子与氯原子结合成氯化钠后体系能量降低 |
| D.在离子化合物CaCl2中,两个氯离子间也存在离子键 |