题目内容
下列分子中,属于含有极性键的非极性分子的是
| A.PCl3 | B.H2S | C.P4 | D.C2H4 |
D
解析试题分析:A.PCl3是分子晶体,含有共价键,分子是三角锥形,正负电荷重心不重合,分子不对称故是极性分子。B.H2S 是V形分子,正负电荷重心不重合,分子不对称故是极性分子,含有极性键。C.P4正负电荷重心重合,分子是正四面体结构,分子对称,故是非极性分子,含有非极性键。D.C2H4含有极性键,正负电荷重心重合,分子对称故是非极性分子,选D。
考点:本题考查分子的极性和化学键类型的判断。

练习册系列答案
相关题目
下列变化需克服共价键的是
| A.金刚石熔化 | B.汞受热变成汞蒸气 | C.蔗糖溶于水 | D.食盐溶于水 |
20世纪80年代后,人们发现并证实了碳的另一类单质,它们是由一系列偶数个碳原子构成的分子,其中C60(足球烯,分子中含有30个双键)最具代表性。下图所示为n个C60连接而成的物质X。下列有关物质X的说法不正确的是( )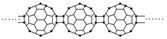
| A.X难溶于水 |
| B.一定条件下X可与H2发生加成反应 |
| C.X的摩尔质量为720n |
| D.X是碳的一种同素异形体 |
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的气态N4分子,其分子结构如右图所示。已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N N放出942 kJ热量,根据以上信息和数据,判断下列说法正确的是
N放出942 kJ热量,根据以上信息和数据,判断下列说法正确的是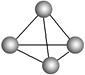
| A.N4属于一种新型的化合物 |
| B.N4分子中存在非极性键 |
| C.N4分子中N—N键角为109°28′ |
| D.1 mol N4转变成N2将吸收882 kJ热量 |
三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如下图所示,已知其燃烧热△H=-3677kJ/mol(P被氧化为P4O10),下列有关P4S3的说法中不正确的是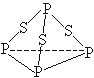
| A.分子中每个原子最外层均达到8电子稳定结构 |
| B.P4S3中硫元素为-2价磷元素为+3价 |
| C.热化学方程式为P4S3( s)+8O2(g)=P4O10(s )+3SO2(g)△H=-3677kJ/mol |
| D.一个P4S3分子中含有三个非极性共价键 |
在预防甲型H1N1流感疫情时,防疫部门使用了含氯类消毒剂,其中的氯胺是一种长效缓释有机氯消毒剂,有强氧化性,其杀菌能力是一般含氯消毒剂的4—5倍,下列有关氯胺(NH2Cl)的说法一定不正确的是( )
| A.氯胺水解产物为NH2OH(羟氨)和HCl |
| B.氯胺的消毒原理与漂白粉相似 |
| C.氯胺中氯的化合价为+1 |
D.氯胺的电子式为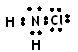 |
下列说法中正确的是
| A.NO2、SO2、BF3分子中所有原子的最外层电子都满足了8e-稳定结构 |
| B.P4和CH4都是正四面体分子且键角都为109o28ˊ |
| C.NaCl晶体中与每个Na+距离相等且最近的Na+共有12个 |
| D.原子间通过共价键而形成的晶体一定具有高的熔、沸点及硬度 |
下列说法中,正确的是( )。
| A.在离子化合物中不可能含有共价键 |
| B.在共价化合物中也可能含有离子键 |
| C.凡含有离子键的化合物一定是离子化合物 |
| D.由不同种非金属元素组成的化合物中只含有极性键 |
下列物质按只含离子键、只含共价键、既含离子键又含共价键的顺序排列的是( )
| A.氯气二氧化碳氢氧化钠 |
| B.氯化钠过氧化氢氯化铵 |
| C.氯化钠过氧化钠氯化铵 |
| D.氯化钠氦气氢氧化钠 |