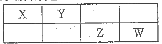
元素X、Y、Z的原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子排布。下列推测不正确的是( )。
| A.同周期元素中X的金属性最强 |
| B.原子半径:X>Y,离子半径:X+>Z2- |
| C.同族元素中Z的氢化物稳定性最高 |
| D.同周期元素中Y的最高价含氧酸的酸性最强 |
有人建议将氢元素排在元素周期表的ⅦA族。下列事实能支持这一观点的是( )。
①H原子得到一个电子实现最外电子层稳定结构;
②氢分子的结构式为H—H;
③与碱金属元素形成离子化合物:M+[:H]-
④分子中原子间的化学键都属于非极性键
| A.①②③ | B.①③④ | C.②③④ | D.①②③④ |
短周期元素X、Y、Z、W,它们的原子序数依次增大。X与Z同主族,并且原子序数之和为20。Y原子的质子数为Z原子的质子数的一半,W原子的最外层电子数比Y原子的最外层电子数多2个。下列叙述正确的是
| A.原子半径Z>W>Y>X |
| B.Y的最高价氧化物对应的水化物可与其气态氢化物发生化合反应 |
| C.气态氢化物的稳定性Z>W |
| D.X的气态氢化物与足量W单质在光照条件下反应生成物均为气体 |
已知短周期元素R、W、X、Y、Z的原子序数依次增大,其氢化物中上述元素的化合价如下表,下列说法正确的是( )
| 元素 | R | W | X | Y | Z |
| 化合价 | –4 | +1 | –4 | –2 | –1 |
A.离子还原性:Y2->Z-
B.离子半径W+>Z-
C.气态氢化物稳定性:RH4<XH4
D.酸性:H2YO4<HZO4
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是( )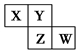
| A.元素W的最高价氧化物对应水化物的酸性最强 |
| B.单核阴离子半径的大小顺序为:r(W)>r(Z) >r(Y) |
| C.元素Y和元素Z的氢化物中均只存在极性共价键 |
| D.元素Y和元素Z的最高正化合价相同 |
X、Y、Z、W为四种短周期元素,有关这四种元素的说法中一定正确的是( )
| 元素 | X | Y | Z | W |
| 原子半径(nm) | 0.077 | 0.075 | 0.102 | 0.099 |
| 最高正价或最低负价 | +4 | +5 | -2 | -1 |
A.X与W形成XW4时,各原子最外层均满 足8电子稳定结构,
B.1molW的单质参加氧化还原反应时转移的电子数为2mol
C.0.3molCu分别与足量HYO3和H2ZO4的稀溶液反应均产生0.2mol气体
D.Y的氢化物与W的氢化物反应的产物只含有共价键
元素周期律和元素周期表是学习化学的重要工具,下列叙述不正确的是( )
| A.从左到右,元素周期表中的第13列为ⅢA族 |
| B.某ⅡA族元素的原子序数为x ,则与它同周期的ⅢA族元素的原子序数可能为x+25 |
| C.ⅥA族元素,随原子半径增大,对应气态氢化物的稳定性逐渐增强 |
| D.53号元素位于周期表P区、第五周期ⅦA族。 |
短周期元素中,原子基态时具有1个未成对电子的元素共有多少种( )
| A.5 | B.6 | C.7 | D.8 |
X和Y是原子序数大于4的短周期元素,Xm+和Yn-两种离子的核外电子排布相同,下
列说法中正确的是( )
| A.X的原子半径比Y小 | B.第一电离能X<Y |
| C.电负性X>Y | D.X和Y的核电荷数之差为m-n |