题目内容
元素周期律和元素周期表是学习化学的重要工具,下列叙述不正确的是( )
| A.从左到右,元素周期表中的第13列为ⅢA族 |
| B.某ⅡA族元素的原子序数为x ,则与它同周期的ⅢA族元素的原子序数可能为x+25 |
| C.ⅥA族元素,随原子半径增大,对应气态氢化物的稳定性逐渐增强 |
| D.53号元素位于周期表P区、第五周期ⅦA族。 |
C
解析试题分析:A、第ⅢA族位于元素周期表从左到右的第13列,正确;B、某ⅡA族元素的原子序数为x ,则与它同周期的ⅢA族元素的原子序数可能是x+1、x+11、x+25,正确;C、ⅥA族元素,随原子半径增大,也即从上到下,对应气态氢化物的稳定性逐渐减弱,错误;D、53号元素的最外层电子排布式为5s25p5,所以位于周期表P区、第五周期ⅦA族,正确,答案选C。
考点:考查元素周期表的排列规律,元素周期律的应用,元素在周期表中位置的判断

练习册系列答案
相关题目
下列说法正确的是
| A.14C与14N互为同位素 | B.葡萄糖与果糖互为同分异构体 |
| C.H2与CH4互为同系物 | D.SO2与SO3互为同素异形体 |
下列电子排布图能表示氮原子的最低能量状态的是( )
A.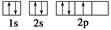 | B.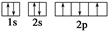 |
C.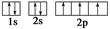 | D. |
1934年居里夫妇用α粒子(4He)轰击27Al得到一种自然界不存在的磷元素的一种同位素(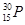 ):
):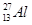 +
+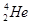 ―→
―→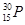 +
+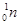 ,开创了人造核素的先河。下列有关说法不正确的是
,开创了人造核素的先河。下列有关说法不正确的是
| A.该变化说明原子核在一般的化学反应中也能发生变化 |
| B.该变化同样遵循质量守恒定律 |
C.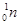 是一种电中性粒子 是一种电中性粒子 |
D.对于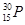 有:原子序数=质子数=中子数=核外电子数 有:原子序数=质子数=中子数=核外电子数 |
下列各原子或离子的电子排布式错误的是( )。
| A.C 1s22s22p2 |
| B.O2- 1s22s22p6 |
| C.Cr 1s22s22p63s23p63d44s2 |
| D.Al3+ 1s22s22p6 |
1913年,丹麦科学家玻尔第一次认识到氢原子光谱是氢原子的电子跃迁产生的。玻尔的原子结构理论一个很大的成就是( )。
| A.证明了原子核外电子在圆形轨道上运动 |
| B.提出了原子核是可以进一步细分的 |
| C.解决了氢原子光谱和原子能级之间的关系 |
| D.应用了量子力学理论中的概念和方法 |
有a、b、c、d四种元素,a、b的阳离子和c、d的阴离子电子层结构相同,已知b的阳离子半径大于a的阳离子半径;c的阴离子比d的阴离子还原能力强,则四种元素的原子序数大小关系是 ( )。
| A.a>b>d>c | B.b>a>c>d | C.b>a>d>c | D.c>b>a>d |
已知X、Y、Z为原子序数相连的三种元素,最高价氧化物对应水化物的酸性相对强弱关系为:HXO4>H2YO4>H3ZO4。则下列说法中正确的是( )
| A.气态氢化物的稳定性:HX>H2Y>ZH3 |
| B.非金属活泼性:Y<X<Z |
| C.原子半径:X>Y>Z |
D.原子最外电子层上的电子数关系:Z=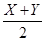 |