题目内容
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是( )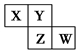
| A.元素W的最高价氧化物对应水化物的酸性最强 |
| B.单核阴离子半径的大小顺序为:r(W)>r(Z) >r(Y) |
| C.元素Y和元素Z的氢化物中均只存在极性共价键 |
| D.元素Y和元素Z的最高正化合价相同 |
A
解析试题分析:Y原子的最外层电子数是其电子层数的3倍,再结合Y在元素周期表的位置可以推测出Y为O元素,从而推测出X、Z、W分别是N、S、Cl,所以比较这四种元素的非金属性可知,Cl的非金属性最强,Cl元素的最高价氧化物对应水化物的酸性最强,A正确;阴离子半径S2->Cl->O2- ,故B错误;O的氢化物有H2O、H2O2两种,所以在H2O2中含有非极性共价键,故C错误;O元素没有正价,故D说法错误;故选A。
考点:本题考查的是元素周期表和元素周期律的性质。

练习册系列答案
相关题目
下列说法正确的是
| A.L层上的电子数为奇数的原子一定是主族元素的原子 |
| B.元素周期表共有18列,第8列属于第ⅧB族、第17列属于第VIIA族 |
| C.化学键的形成一定伴随着电子的转移和能量变化 |
| D.元素周期表中,位于金属和非金属交界线附近的元素属于过渡元素 |
根据元素周期律和物质结构的有关知识,以下有关排序错误的是( )
| A.离子半径:S2->Cl->Ca2+ | B.原子半径:Ca>S>Cl |
| C.酸性:HClO4<HBrO4<HIO4 | D.热稳定性:HCl>H2S>H2Se |
下列基态原子的电子排布式中,其未成对电子数最多的是( )
| A.1s22s22p63s23p63d54s1 |
| B.1s22s22p63s23p3 |
| C.1s22s22p63s23p63d64s2 |
| D.1s22s22p63s23p63d74s2 |
下列说法正确的是
| A.第ⅠA族元素的金属性比第ⅡA族元素的金属性强 |
| B.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
| C.同周期非金属氧化物对应水化物的酸性从左到右依次增强 |
| D.第3周期元素的离子半径从左到右逐渐减小 |
下列各原子或离子的电子排布式错误的是( )。
| A.K+ 1s22s22p63s23p6 |
| B.F 1s22s22p5 |
| C.S2- 1s22s22p63s23p4 |
| D.Ar 1s22s22p63s23p6 |
元素X、Y、Z的原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子排布。下列推测不正确的是( )。
| A.同周期元素中X的金属性最强 |
| B.原子半径:X>Y,离子半径:X+>Z2- |
| C.同族元素中Z的氢化物稳定性最高 |
| D.同周期元素中Y的最高价含氧酸的酸性最强 |
下列说法中肯定错误的是 ( )。
| A.某原子K层上只有一个电子 |
| B.某原子M层上电子数为L层电子数的4倍 |
| C.某离子M层上和L层上的电子数均为K层的4倍 |
| D.某离子的核电荷数与最外层电子数相等 |
如图是短周期元素周期表的一部分,下列说法中正确的是( )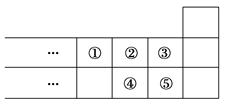
| A.元素①位于第二周期第ⅣA族 |
| B.气态氢化物的稳定性:④>② |
| C.最高价氧化物对应水化物的酸性:⑤>④ |
| D.元素的最高正化合价:③=⑤ |