题目内容
X和Y是原子序数大于4的短周期元素,Xm+和Yn-两种离子的核外电子排布相同,下
列说法中正确的是( )
| A.X的原子半径比Y小 | B.第一电离能X<Y |
| C.电负性X>Y | D.X和Y的核电荷数之差为m-n |
B
解析试题分析:Xm+和Yn-两种离子的核外电子排布相同,根据“阴上阳下”的原则,X在第三周期,Y在第二周期。A、X的原子半径大于Y,错误;B、X是第三周期偏左的位置,Y是第二周期偏右的位置,根据第一电离能的变化规律,周期表中一般偏左下的元素的第一电离能较小,正确;C、根据电负性的判断依据,周期表中偏右上的元素的电负性较大,所以应是Y>X,错误;D、X和Y的核电荷数之差为m+n,错误,答案选B。
考点:考查元素在周期表中的位置与元素周期律的关系

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案X、Y、Z、W是前20号元素,原子序数依次增大。X是原子半径最小的元素;Y元素原子的最外层电子数是电子层数的2倍;Z元素的-1价阴离子的核外电子排布与氖原子相同,W元素为金属,它的某种化合物可用于烟气脱硫。下列说法错误的是
| A.X、Y形成的化合物中可能含有双键 |
| B.X单质和Z单质在暗处能剧烈反应 |
C.W元素与Z元素形成的化合物用电子式表示形成过程为: |
| D.XZ的沸点在与Z同族的其它X的化合物中最高 |
已知短周期元素R、W、X、Y、Z的原子序数依次增大,其氢化物中上述元素的化合价如下表,下列说法正确的是( )
| 元素 | R | W | X | Y | Z |
| 化合价 | –4 | +1 | –4 | –2 | –1 |
A.离子还原性:Y2->Z-
B.离子半径W+>Z-
C.气态氢化物稳定性:RH4<XH4
D.酸性:H2YO4<HZO4
元素周期律产生的根本原因就是随着元素原子序数的递增
| A.元素的相对原子质量逐渐增大 |
| B.核外电子排布呈周期性变化 |
| C.原子半径呈周期性变化 |
| D.元素主要化合价呈周期性变化 |
各电子层排布电子的总数遵循以下规则:①每层最多容纳2n2个电子;②原子最外层电子数≤8;③原子次外层电子数≤18。决定这3条规律的电子排布规则是( )。
| A.能量最低原则 |
| B.泡利不相容原理 |
| C.洪特规则 |
| D.能量最低原则和泡利不相容原理 |
关于原子模型的演变过程,正确的是( )。
| A.汤姆逊原子模型→道尔顿原子模型→卢瑟福原子模型→玻尔原子模型→量子力学模型 |
| B.汤姆逊原子模型→卢瑟福原子模型→玻尔原子模型→量子力学模型→道尔顿原子模型 |
| C.道尔顿原子模型→卢瑟福原子模型→汤姆逊原子模型→玻尔原子模型→量子力学模型 |
| D.道尔顿原子模型→汤姆逊原子模型→卢瑟福原子模型→玻尔原子模型→量子力学模型 |
X、Y和Z是短周期的三种元素,已知X元素原子的最外层只有一个电子,Y元素原子M层上的电子数是K层和L层电子总数的一半,Z元素原子L层上的电子数比Y元素原子L层上电子数少2个,则这三种元素所组成的化合物的化学式不可能是( )。
| A.X2YZ4 | B.XYZ3 | C.X3YZ4 | D.X4Y2Z7 |
某粒子结构示意图为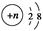 ,若该粒子为离子,则它所带的电荷数可能为( )。
,若该粒子为离子,则它所带的电荷数可能为( )。
①8-n ②n-8 ③10-n ④n-10
| A.①② | B.①③ | C.③④ | D.②④ |
对四种元素G、L、M、R进行如下实验:
| 金属 实验 | G | L | M | R |
| 和冷水反应 | 不反应 | 慢慢反应 | 未做实验 | 未做实验 |
| 和2 mol·L-1 盐酸反应 | 溶解并放 出气体 | 溶解并 放出气体 | 不反应 | 不反应 |
| 和Rn+的 水溶液反应 | 溶解并形 成沉淀 | 未做实验 | 溶解并 形成沉淀 | 未做实验 |
根据表中所给实验结果,判断这四种金属活泼性由强到弱的顺序正确的是( )
A.L、G、R、M B.G、L、M、R
C.L、G、M、R D.L、R、G、M