将20 mL NO2和NH3的混合气体,在一定条件下充分反应,化学方程式为: 6NO2+8NH3=7N2+12H2O,已知参加反应的NO2比参加反应的NH3少2 mL(气体体积均在相同状况下测定),则原混合气体中NO2和NH3的物质的量之比是( )
①3:2 ②2:3 ③3:7 ④3:4
| A.①③ | B.②④ | C.①② | D.③④ |
下列陈述正确并且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | 浓硫酸有强氧化性 | 浓硫酸可用于干燥H2和CO |
| D | Fe3+有强氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
下列对事实的解释不正确的是
| 选项 | 事实 | 解释 |
| A | 用铝罐槽车储运浓硫酸 | 浓硫酸的强氧化性使铝钝化 |
| B | 用饱和NH4Cl溶液处理过的舞台布帘可防火 | NH4Cl分解吸热,且分解产物能隔绝空气中的氧气 |
| C | 钠元素的焰色反应呈黄色 | Na2O2是一种淡黄色的固体 |
| D | SO2能使溴水褪色 | SO2具有还原性 |
下列有关硅及其化合物的说法正确的是
| A.单质硅常用作半导体和光导纤维材料 |
| B.硅在自然界中只以化合态的形式存在 |
| C.SiO2与纯碱高温生成CO2,说明硅酸的酸性比碳酸强 |
| D.SiO2是非金属氧化物,它不与任何酸反应 |
氯气是一种重要的工业原料。工业上利用反应在3Cl2+8NH3=N2+6NH4Cl检查氯气管道是否漏气。下列说法正确的是
| A.若管道漏气遇氨就会产生白雾 | B.该反应利用了氨气的还原性 |
| C.该反应属于复分解反应 | D.生成6molNH4Cl有18mol电子转移 |
叠氮酸钠(NaN3)是无色离子晶体,遇高温或剧烈震动能发生强烈爆炸,快速分解成钠单质和氮气,是汽车安全气囊中的成分之一。下列有关说法正确的是
| A.NaN3中只含有离子键 |
| B.1molNaN3完全分解最多可以产生33.6LN2 |
| C.NaN3快速分解时,NaN3既是氧化剂,又是还原剂 |
| D.常温下,NaN3化学性质稳定,包装盒上无需特别说明注意事项 |
N、O、Si、S是重要的非金属元素,下列说法正确的是
| A.N、O、S、Si的原子半径逐渐增大,非金属性逐渐减弱 |
| B.氮的氧化物和硫的氧化物既是形成光化学烟雾,又是形成酸雨的主要物质 |
| C.S、SO2和Si、SiO2四种物质均能与NaOH溶液反应,各自又能与某些酸反应 |
| D.N、Si、S的单质均能和氧气反应,生成的产物分别是NO2、SiO2和SO2 |
有科学家预测,氨能有望取代氢能,成为重要的新一代绿色能源。下列有关说法不正确的是( )
| A.液氨作为清洁能源的反应原理是4NH3+5O2=4NO+6H2O |
| B.液氨具有腐蚀性和毒性,在使用过程中要防止氨泄漏 |
| C.氨气比空气轻,标准状况下密度约为0.76g·L-1 |
| D.氨与氢气相比,优点在于氨不容易发生爆炸,使用时更安全 |
下列说法正确的是( )
| A.硫粉在过量的氧气中燃烧可以生成SO3 |
| B.可以用澄清石灰水鉴别CO2和SO2 |
| C.将少量CO2通入BaCl2溶液能生成白色沉淀 |
| D.不能用排水法收集SO2、NO2气体 |
硝酸铜是制备Cu—Zn—Al系催化剂的重要原料。现有三种制取硝酸铜的实验方案可供选用:①铜与稀硝酸反应制取:3Cu + 8HNO3(稀)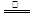 3Cu(NO3)2 + 2NO↑+ 4H2O
3Cu(NO3)2 + 2NO↑+ 4H2O
②铜与浓硝酸反应制取:Cu + 4HNO3(浓)= Cu(NO3)2 + 2NO2↑+ 2H2O
③首先将铜屑在空气中加热生成氧化铜,氧化铜与稀硝酸反应制取:2Cu + O2 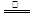 2CuO,CuO + 2HNO3 = Cu(NO3)2 + H2O 下列有关说法正确的是( )
2CuO,CuO + 2HNO3 = Cu(NO3)2 + H2O 下列有关说法正确的是( )
| A.制取等量的硝酸铜,需硝酸的量②最少 |
| B.制取等量的硝酸铜,②产生的有毒气体比①少 |
| C.三种方案中,第③方案最经济环保 |
| D.三种方案的反应都可以在铁质容器中进行 |