下列溶液中c(Cl-)与50 mL 1 mol/LAlCl3溶液中c(Cl-)相等的是
| A.150 mL 1 mol/L的NaCl溶液 | B.75 mL 2 mol/L的NH4Cl溶液 |
| C.150 mL 2 mol/L的KCl溶液 | D.75 mL 1 mol/L的FeCl3溶液 |
下列数量的物质中含原子数最多的是
| A.4℃时5.4mL水 | B.标准状况下5.6L二氧化碳 |
| C.0.4mol氧气 | D.10g氖 |
物质的量相等的两种气体,必然
| A.分子数相同 | B.均为22.4L |
| C.原子数相同 | D.体积相同 |
下列叙述正确的是
| A.3.01×1023个SO2分子的质量为32g |
| B.CH4的摩尔质量为16g |
| C.1 mol H2O的质量为18g/mol |
| D.标准状况下,1 mol任何物质体积均为22.4L |
向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系不正确的是
| A.c=1000b/11.2V | B.p=m+Vc/125 | C.n=m+17Vc | D.5/3m<p<17/9m |
设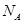 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
A.1.7gH2O2中含有的中子数目为0.9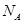 |
B.1molNa2O2固体中含离子总数为4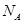 |
C.标准状况下,0.1molCl2溶于水,转移电子数目为0.1 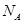 |
D.25℃,pH=13的NaOH溶液中含有OH-的数目为0.1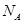 |
设NA为阿伏加德罗常数,则下列说法正确的是
| A.电解精炼铜时,若阴极得到电子数为2 NA,阳极质量减少64g |
| B.200mL某硫酸盐溶液中含有1.5 NA个SO42-离子,同时含有NA个金属阳离子,该盐物质的量浓度是2.5 mol/L |
| C.常温常压下,78g Na2O2固体中所含阴、阳离子总数为4 NA |
| D.一定条件下,足量的Fe粉与浓硫酸反应,转移电子数一定为2 NA |
NA代表阿伏加德罗常数的值。下列叙述正确的是
A.1mol 分子中含共价键总数为6NA 分子中含共价键总数为6NA |
| B.7.8gNa2O2与CO2完全反应转移电子数为0.2NA |
| C.300mL 2mol/L蔗糖溶液中所含分子数为0.6NA |
| D.常温下,20L pH=12的Na2CO3溶液中含有OH-数目为0.2NA |
铁和氧化铁的混合物共a mol,加盐酸后固体全部溶解,共收集到b mol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中铁的物质的量为
A. (a+b) mol (a+b) mol | B.(a-b) mol | C. (a-b)mol (a-b)mol | D.(a+b) mol |
将a g二氧化锰粉末加入b mol/L的浓盐酸c L中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,下列叙述正确的是
A.可以收集到氯气 L L |
B.反应后溶液中的Cl―数目为: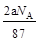 |
C.NA可表示为: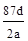 |
D.反应后溶液中的H+数目为: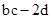 |