题目内容
物质的量相等的两种气体,必然
| A.分子数相同 | B.均为22.4L |
| C.原子数相同 | D.体积相同 |
A
解析试题分析:根据阿伏伽德罗定律,物质的量相等的两种气体分子数一定相等,因为温度、压强等外界条件不确定,所以体积大小不能确定,气体分子所含原子数不一定相等,所以两种气体的原子数不一定相等,故A项正确。
考点:本题考查阿伏伽德罗定律。

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
以NA为阿伏加德罗常数的值,下列说法正确的是( )
| A.标准状况下,22.4L的H2和CO2混合气体中含有的分子总数为NA |
| B.常温常压下,24g金属镁变为镁离子时得到的电子数为2NA |
| C.标准状况下,5.6L水含有的分子数为0.25NA |
| D.1 mol Cl2与足量Fe反应,转移的电子数为3NA |
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是
A.次氯酸的电子式: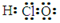 |
B.质量数为16的氧原子: |
C.乙烯的结构简式: |
D.碳酸氢根离子的电离方程式: HCO3-+ H2O H3O++ CO32- H3O++ CO32- |
NA代表阿伏加德罗常数的值。下列叙述正确的是
A.1mol 分子中含共价键总数为6NA 分子中含共价键总数为6NA |
| B.7.8gNa2O2与CO2完全反应转移电子数为0.2NA |
| C.300mL 2mol/L蔗糖溶液中所含分子数为0.6NA |
| D.常温下,20L pH=12的Na2CO3溶液中含有OH-数目为0.2NA |
在无土栽培液中,每升溶液需用0.98mol NH4Cl溶液、0.16 mol KCl溶液、0.24molK2SO4溶质作为培养液,若用KCl、NH4Cl和(NH4)2SO4三种物质来配制1.00L上述营养液,所需三种盐的物质的量是
| A.0.4mol、0.5mol、0.12mol |
| B.0.66mol、0.5mol、0.24mol |
| C.0.64mol、0.5mol、0.24mol |
| D.0.64mol、0.02mol、0.24mol |
下列化学用语正确的是
A.硫离子的结构示意图: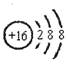 |
B.氟化镁的电子式: |
| C.甘氨酸的结构式:C2H5O2N |
| D.氢氧化钡的电离方程式:Ba(OH)2=Ba2++(OH)22- |
下列化学用语表示正确的是
A.CO2的比例模型: |
B.铝离子的结构示意图: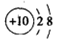 |
| C.次氯酸的结构式:H-Cl-O |
D.甲基的电子式: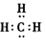 |
相同质量的两份铝,分别放入足量的盐酸和氢氧化钠溶液中,放出的氢气在同温同压下的体积之比为
| A.1:1 | B.1:6 | C.2:3 | D.3:2 |