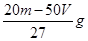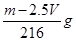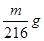设NA为阿伏加德罗常数的值,下列说法正确的组合是 ( )
a 12 g 金刚石中含有的碳碳键的数目为2NA
b 1 mol 明矾与水完全反应转化为氢氧化铝胶体后,其中胶体粒子的数目为NA
c 标准状况下,2.24L乙烯和丙烯等物质的量混合气体中含有的共用电子对的数目为0.75NA
d 常温下,1 mol·L-1的NH4NO3溶液中含有氮原子的数目为2 NA
e 标准状况下,2.24 L C6H14含原子总数大于2NA
f 17g H2O2中含有的电子数为9NA
g 将2mol SO2与1mol O2混合,发生反应转移的电子总数一定是4NA
h 常温下,100mL 1mol ? L-1 AlCl3溶液中阳离子总数大于0.1NA
| A.a c f h | B.a c e g | C.a c e f h | D.b d e h |
下列选项中所涉及的两个量一定相等的是
| A.11.2 L N2与14 g CO气体所含有的原子数 |
| B.电解精炼铜时阳极溶解与阴极析出的铜的质量 |
| C.6.2 g Na2O和7.8 g Na2O2中所含的离子数 |
| D.18 g重水(D2O)与17 g NH4+所含有的电子数 |
用98%的浓硫酸(密度为1.84g/cm3配制100mL 1 mol/L的稀硫酸,现给出下列仪器(配制过程中可能用到):①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒,配制中使用仪器的先后顺序排列正确的是( )
| A.④③⑦⑤⑥ | B.②⑤⑦⑥ | C.①③⑤⑥⑦ | D.②⑥③⑦⑤⑥ |
用NA表示阿伏加德罗常数的值。下列判断错误的是( )
| A.NA个H+的质量为1 g |
| B.2 L 0.5mol/LNa2SO4溶液中含NA个Na+ |
| C.32 g O2中含有2NA个O原子 |
| D.标准状况下,1 mol H2O中含有NA个分子 |
如图所示,常温常压下气体X(见选项)与O2等物质的量混合后充满圆底烧瓶,挤压胶头滴管并打开止水夹,可观察到烧杯中的水沿导管进入烧瓶。长时间充分反应后,烧瓶中所得溶液的物质的量浓度最小的是(假设溶质不向烧瓶外扩散)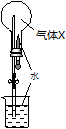
| A.NH3 | B.HCl | C.SO2 | D.NO2(假设不含N2O4) |
含有1mol HNO3的稀硝酸分别与不同物质的量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断正确的是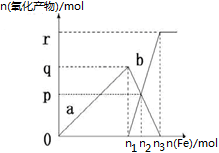
| A.a是Fe(NO3)2 | B.n1=0.375 | C.p=0.20 | D.n2=0.30 |
设NA为阿伏加德罗常数的值,则下列说法正确的是( )
A.常温下,0.1 mol碳酸钠晶体中含有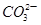 的数目小于0.1 NA 的数目小于0.1 NA |
| B.36gCaO2中含有的离子数目为0.15 NA |
| C.100 g 98%的浓硫酸中,氧原子总数为4NA |
| D.标准状况下,14.2 g氯气与足量石灰乳充分反应转移电子数为0.2NA |
向60 mL Na2SO4溶液中加入BaCl2溶液,有关数据见下表: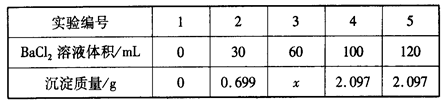
下列有关说法不正确的是
| A.混合前,BaCl2溶液的物质的量浓度为0.10 mol·L-1 |
| B.混合前,Na2SO4溶液的物质的量浓度为0.15 mol·L-1 |
| C.3号实验中沉淀的质量x为1.398 g |
| D.完全沉淀60 mL Na2SO4溶液消耗BaCl2溶液的体积为80 mL |
设NA为阿伏加德罗常数的值。下列说法正确的是
A.在反应5NH4NO3  2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为10NA 2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为10NA |
| B.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
| C.标准状况下,1.12L的SO3所含的原子数约为0.2NA |
| D.标准状况下,2.2gCO2气体中所含分子数为0.05NA |