向含铜粉的硝酸亚铁溶液中滴加足量稀硫酸,下列说法正确的是( )
| A、能反应,但不产生气体 | B、铜粉完全溶解 | C、实验过程中溶液会变色 | D、铜粉不会溶解 |
取铁和铜的混合粉末13.2g,加入100mL 4mol/L的FeCl3溶液中,充分反应后剩余固体2.0g,则混合粉末中Fe的质量可能为( )
| A、13g | B、12g | C、11g | D、2g |
查阅资料:CaO、MgO在高温下与C难反应,但能与SiO2反应.硫铁矿烧渣是一种工业废渣(含Fe2O3及少量SiO2、Al2O3、CaO、MgO等杂质),该烧渣可用于制取氧化铁,具体化工生产工艺流程如下:
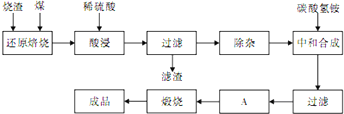
(1)焙烧时产生的主要有害气体是 .
(2)为测定过滤所得滤液中Fe2+的含量,实验室中常用酸性高锰酸钾溶液进行滴定,写出该反应的离子方程式: ;实验中所用酸性高锰酸钾溶液浓度为0.10mol/L,滤液用 滴定管量取20.00ml,用酸性高锰酸钾溶液滴定到终点时消耗了标准的酸性高锰酸钾溶液12.04ml,滤液中c(Fe2+)= .
(3)若在空气中“酸浸”时间过长,溶液中Fe2+含量将下降,其原因是: (用离子方程式表示).
(4)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于 ,检验Fe3+已经除尽的试剂是 (除KSCN外).
(5)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则A的操作是 .

(1)焙烧时产生的主要有害气体是
(2)为测定过滤所得滤液中Fe2+的含量,实验室中常用酸性高锰酸钾溶液进行滴定,写出该反应的离子方程式:
(3)若在空气中“酸浸”时间过长,溶液中Fe2+含量将下降,其原因是:
(4)根据下表数据:
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 3.10 | 2.01 | 7.11 |
| 万全沉淀的pH | 4.77 | 3.68 | 9.61 |
(5)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则A的操作是
Fe2O3具有广泛的用途.
甲同学阅读有关资料得知:在高温下煅烧FeCO3可以得到Fe2O3.为了进一步验证此结论,他做了如下实验:
由此甲同学得出结论:4FeCO3+O2
2Fe2O3+4CO2
(1)写出实验步骤Ⅲ中发生反应的离子方程式 .
(2)乙同学提出了不同的看法:煅烧产物可能是Fe3O4,因为Fe3O4也可以溶于硫酸,且所得溶液中也含有Fe3+.于是乙同学对甲同学的实验步骤Ⅲ进行了补充改进:检验实验步骤Ⅱ所得溶液中是否含有Fe2+.他需要选择的试剂是 (填序号).
a.氯水 b.氯水+KSCN溶液 c.K3[Fe(CN)6](铁氰化钾溶液)
(3)丙同学认为即使得到了乙同学预期的实验现象,也不能确定煅烧产物的成分.你认为丙同学持此看法的理由是 .
(4)丙同学进一步查阅资料得知,煅烧FeCO3的产物中,的确含有+2价铁元素.于是他设计了另一种由FeCO3制取Fe2O3的方法:先向FeCO3中依次加入试剂:稀硫酸、 (填名称)和 (填名称);再 (填操作名称),灼烧,即可得到Fe2O3.
0 59830 59838 59844 59848 59854 59856 59860 59866 59868 59874 59880 59884 59886 59890 59896 59898 59904 59908 59910 59914 59916 59920 59922 59924 59925 59926 59928 59929 59930 59932 59934 59938 59940 59944 59946 59950 59956 59958 59964 59968 59970 59974 59980 59986 59988 59994 59998 60000 60006 60010 60016 60024 203614
甲同学阅读有关资料得知:在高温下煅烧FeCO3可以得到Fe2O3.为了进一步验证此结论,他做了如下实验:
| 实验步骤 | 实验操作 |
| I | 取一定质量的FeCO3固体置于坩埚中,高温燃烧至质量不再减轻,冷却至室温. |
| II | 取少量实验步骤I所得固体放于一洁净的试管中,用足量的稀硫酸溶解. |
| III | 向实验步骤II所得溶液中滴加KSCN溶液,溶液变红. |
| ||
(1)写出实验步骤Ⅲ中发生反应的离子方程式
(2)乙同学提出了不同的看法:煅烧产物可能是Fe3O4,因为Fe3O4也可以溶于硫酸,且所得溶液中也含有Fe3+.于是乙同学对甲同学的实验步骤Ⅲ进行了补充改进:检验实验步骤Ⅱ所得溶液中是否含有Fe2+.他需要选择的试剂是
a.氯水 b.氯水+KSCN溶液 c.K3[Fe(CN)6](铁氰化钾溶液)
(3)丙同学认为即使得到了乙同学预期的实验现象,也不能确定煅烧产物的成分.你认为丙同学持此看法的理由是
(4)丙同学进一步查阅资料得知,煅烧FeCO3的产物中,的确含有+2价铁元素.于是他设计了另一种由FeCO3制取Fe2O3的方法:先向FeCO3中依次加入试剂:稀硫酸、
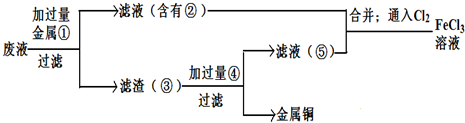

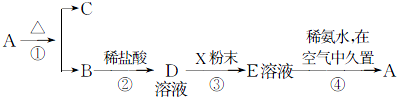
 (1)现有含Fe2O380%的赤铁矿100t,理论上可冶炼含Fe95%的生铁多少吨?
(1)现有含Fe2O380%的赤铁矿100t,理论上可冶炼含Fe95%的生铁多少吨?