题目内容
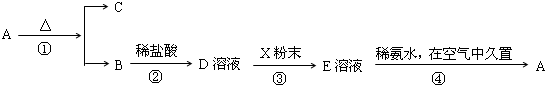
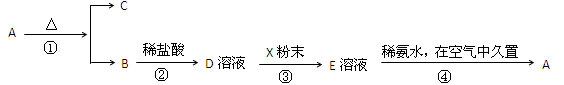
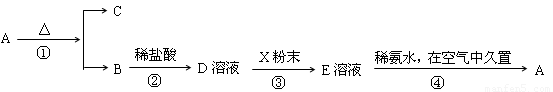
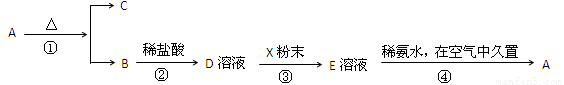
固体化合物A,按下图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色.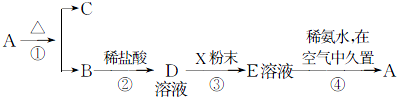
(1)写出下列物质的化学式:
A:
(2)写出反应①的化学方程式:
分析:固体化合物A,按下图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色,B到D时加入的盐酸,推断E为FeCl2,A为Fe(OH)3,A加热分解生成B为Fe2O3,C为H2O,依据流程分析判断D为FeCl3,X为Fe,E为FeCl2溶液,依据分析推断出的物质分析回答.
解答:解:已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色说明A为氢氧化铁Fe(OH)3,A加热分解生成B为Fe2O3,C为H2O,依据流程分析判断D为FeCl3,X为Fe,E为FeCl2溶液,
(1)依据推断可知A为Fe(OH)3,B为Fe2O3,C为H2O,D为FeCl3,E为FeCl2,X为Fe;
故答案为:Fe(OH)3;Fe2O3;FeCl3;FeCl2;Fe;
(2)反应①是氢氧化铁分解生成氧化铁和水的反应,反应为2Fe(OH)3
Fe2O3+3H2O;
反应②是盐酸和氧化铁发生的复分解反应,反应为Fe2O3+6HCl=2FeCl3+3H2O;
反应③是氯化铁和铁发生的氧化还原反应,反应为Fe+2FeCl3=3FeCl2,离子方程式为2Fe3++Fe═3Fe2+;
反应④是氢氧化亚铁和氧气水 发生反应生成氢氧化铁的也还原反应,反应化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3;
故答案为:2Fe(OH)3
Fe2O3+3H2O;2Fe3++Fe═3Fe2+;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(1)依据推断可知A为Fe(OH)3,B为Fe2O3,C为H2O,D为FeCl3,E为FeCl2,X为Fe;
故答案为:Fe(OH)3;Fe2O3;FeCl3;FeCl2;Fe;
(2)反应①是氢氧化铁分解生成氧化铁和水的反应,反应为2Fe(OH)3
| ||
反应②是盐酸和氧化铁发生的复分解反应,反应为Fe2O3+6HCl=2FeCl3+3H2O;
反应③是氯化铁和铁发生的氧化还原反应,反应为Fe+2FeCl3=3FeCl2,离子方程式为2Fe3++Fe═3Fe2+;
反应④是氢氧化亚铁和氧气水 发生反应生成氢氧化铁的也还原反应,反应化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3;
故答案为:2Fe(OH)3
| ||
点评:本题考查了铁及其化合物性质的分析判断,物质转化关系和特征反应的分析应用是解题关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目