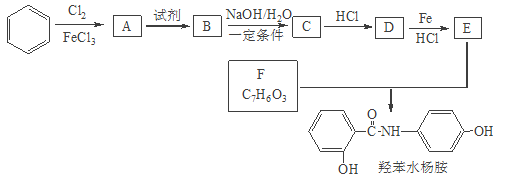
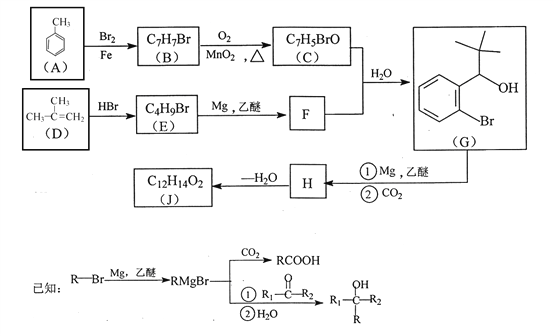
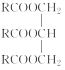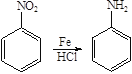【题目】FeCl2是一种用途广泛的化工产品。由于在水溶液中难以得到高纯度的FeCl2,某课题小组设计氯化铁和氯苯反应制得高纯度的FeCl2。
(查阅资料)①在加热条件下,氯化铁遇水剧烈水解。
②2FeCl3 +C6H5Cl →C6H4Cl2 + 2FeCl2 + HCl↑
③有关数据如下:
C6H5Cl(氯苯) | C6H4Cl2(对二氯苯) | FeCl3 | FeCl2 | |
式量 | 112.5 | 147 | 162.5 | 127 |
溶解性 | 不溶于水,易溶于苯 | 溶于水,不溶于C6H5Cl、C6H4Cl2、苯 | ||
熔点/℃ | -45 | 53 | —— | —— |
沸点/℃ | 132 | 173 | —— | —— |
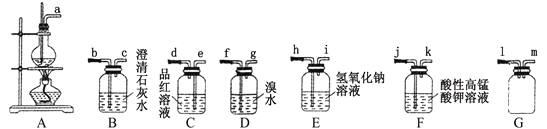
(实验过程)按下图装置,在三颈烧瓶中放入a g无水氯化铁和过量的氯苯,控制反应温度在128~139℃加热3h,冷却,分离提纯A中物质得到产品。
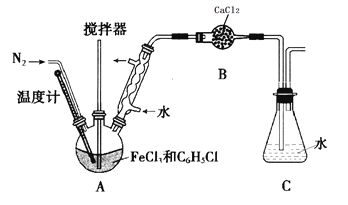
回答下列问题:
(1)实验装置中,仪器B的名称是________________。
(2)反应前后都需要通入N2的目的是_____________。
(3)实验过程中控制反应温度128~139℃,C6H5Cl不会有明显损失,原因是_____________。
(4)充分反应后,冷却。对三颈烧瓶内的物质进行过滤,用苯洗涤沉淀,干燥得到产品。回收滤液中C6H5Cl的方案为_______________。
(5)经检验产品中不含有FeCl3。取少量所得产品溶解于盐酸中,配制成溶液。向盛有H2O2溶液的试管中加入几滴配制的溶液,溶液变成棕黄色,一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是__________;生成沉淀的原因是(用平衡移动原理解释)__________。
【题目】乙酸正丁酯是医药合成的重要中间体,某同学在实验室中用乙酸和正丁醇来制取,实验操作如下:
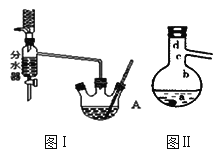
Ⅰ.将混合液(18.5 mL正丁醇和13.4 mL过量乙酸,0.4 mL浓硫酸)置于仪器A中并放入适量沸石(见图I,沸石及加热装置等略去),然后加热回流约20分钟。
Ⅱ.将反应后的溶液进行如下处理:①用水洗涤,②用试剂X干燥,③用10% Na2CO3溶液洗涤。
Ⅲ.将所得到的乙酸正丁酯粗品转入蒸馏烧瓶中进行蒸馏,最后得到17.1 g乙酸正丁酯。
部分实验数据如下表所示:
化合物 | 相对分子质量 | 密度/(g·mL-1) | 沸点/℃ | 溶解度(g)/(100 g水) |
正丁醇 | 74 | 0.80 | 118.0 | 9 |
乙酸 | 60 | 1.045 | 118.1 | 互溶 |
乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
(1)使用分水器(实验中可分离出水)能提高酯的产率,其原因是_______________.
(2)步骤Ⅱ中的操作顺序为____________(填序号),试剂X不能选用下列物质中的______________(填字母序号)。
a.无水硫酸镁 b.新制生石灰 c.无水硫酸钠
(3)步骤Ⅲ(部分装置如图Ⅱ所示)。
①当仪器连接好后,a.向相应的冷凝管中通冷凝水;b.加热蒸馏烧瓶,先后顺序是___________。(填“先a后b”或“先b后a”)
②温度计水银球所处的位置不同,会影响馏出物的组成,当温度计水银球分别位于图Ⅱ中的________(填“a”“b”“c”或“d”)点时会导致收集到的产品中混有较多的低沸点杂质。
(4)该实验乙酸正丁酯的产率是_____________。(计算结果保留2位有效数字)。