9.往含Fe3+、H+、NO3-的混合液中加入少量SO${\;}_{3}^{2-}$,充分反应后,下列表示该反应的离子方程式正确的是( )
| A. | 2Fe3++SO${\;}_{3}^{2-}$+H2O═2Fe2++SO${\;}_{4}^{2-}$+2H+ | |
| B. | 2H++SO${\;}_{3}^{2-}$═H2O+SO2↑ | |
| C. | 2H++2NO${\;}_{3}^{-}$+3SO${\;}_{3}^{2-}$═3SO${\;}_{4}^{2-}$+2NO↑+H2O | |
| D. | 2Fe3++3SO${\;}_{3}^{2-}$+3H2O═2Fe(OH)3↓+3SO2↑ |
7.将2.3g钠放入97.7g水中,下列说法正确的是( )
| A. | 产生的气体含有0.1mol的电子 | B. | 电子转移的数目为2NA | ||
| C. | 所得溶液的质量分数是等于4% | D. | 产生气体的体积为1.12L |
6.元素${\;}_{8}^{18}$O的原子核内中子数与质子数之差为( )
| A. | 8 | B. | 10 | C. | 2 | D. | 18 |
4.对于下列物质中制定元素化合价分析错误的是( )
| A. |  | B. |  | C. |  | D. |  |
3.在下列变化中,需加入氧化剂才能进行的是( )
0 173652 173660 173666 173670 173676 173678 173682 173688 173690 173696 173702 173706 173708 173712 173718 173720 173726 173730 173732 173736 173738 173742 173744 173746 173747 173748 173750 173751 173752 173754 173756 173760 173762 173766 173768 173772 173778 173780 173786 173790 173792 173796 173802 173808 173810 173816 173820 173822 173828 173832 173838 173846 203614
| A. | KMnO4→MnO2 | B. | Na2CO3→CO2 | C. | Fe2+→Fe | D. | CO→CO2 |
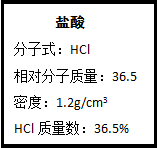 图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题: