13.把3molA和2.5molB混合盛入容积为2L的容器内,使它们发生反应:3A(气)+B(气)?xC(气)+2D(气)经过5min后达到平衡生成1mol D,测得C的平均生成速率为0.10mol•L-1•min-1.下列叙述正确的是( )
| A. | A的平均消耗速率为0.32mol•L-1•min-1 | |
| B. | B的转化率为80% | |
| C. | x的值为2 | |
| D. | B的平衡浓度为1mol•L-1 |
12.有甲、乙、丙三瓶等体积、等物质的量浓度的硫酸.若将甲用水稀释,乙中加入适量的BaCl2溶液,丙不变,然后用等浓度的NaOH溶液中和,至完全反应时,所需NaOH溶液的体积是( )
| A. | 丙>乙>甲 | B. | 甲=丙>乙 | C. | 乙>丙>甲 | D. | 甲=乙=丙 |
11.下列说法正确的是( )
| A. | 澄清石灰水可用来鉴别Na2CO3和NaHCO3溶液 | |
| B. | 能使湿润的碘化钾淀粉试纸变蓝的物质一定是氯气 | |
| C. | NO2、CO2和SO2溶于水均可导电,它们都是电解质 | |
| D. | 将SO2通入酸化的Ba(NO3)2溶液中会出现白色沉淀 |
10.下列关于实验的叙述合理的是( )
| A. | 某氢化物的溶液能使石蕊试液变蓝,该氢化物一定是氨气 | |
| B. | 在Fe(OH)3胶体中和Fe(NO3)3溶液中分别逐滴加入HI稀溶液至过量,整个过程中现象相同 | |
| C. | 配制硫酸亚铁溶液时应将硫酸亚铁固体溶于浓硫酸中,再稀释至所需浓度,以防止水解 | |
| D. | 酸性高锰酸钾溶液、品红溶液、硫化钠溶液都能将SO2和CO2气体区别开 |
9.下列说法正确的是( )
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | a molH2O和a molCO2所含分子数目相同 | |
| C. | 1mol氦气含有的氦原子物质的量是2mol | |
| D. | 摩尔是国际单位制中七个物理量之一 |
8.在恒温、恒容条件下发生下列反应:2X2O5(g)═4XO2(g)+O2(g)△H>0,T温度下的部分实验数据为:
下列说法不正确的是( )
| t/s | 0 | 50 | 100 | 150 |
| c(X2O5)mol/L | 4.00 | 2.50 | 2.00 | 2.00 |
| A. | T温度下的平衡常数为K=64(mol/L)3,100s时转化率为50% | |
| B. | 50s内X2O5分解速率为0.03 mol/(L•s) | |
| C. | T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1>K2 | |
| D. | 若只将恒容改为恒压,其它条件都不变,则平衡时X2O5的转化率和平衡常数都不变 |
6.下列叙述中,正确的是( )
0 173353 173361 173367 173371 173377 173379 173383 173389 173391 173397 173403 173407 173409 173413 173419 173421 173427 173431 173433 173437 173439 173443 173445 173447 173448 173449 173451 173452 173453 173455 173457 173461 173463 173467 173469 173473 173479 173481 173487 173491 173493 173497 173503 173509 173511 173517 173521 173523 173529 173533 173539 173547 203614
| A. | 依据铝热反应原理,能发生反应2Al+3MgO$\frac{\underline{\;高温\;}}{\;}$3Mg+Al2O3 | |
| B. | 在加入铝粉能放出氢气的溶液中:K+、NH4+、CH3COO-、Cl-一定能够大量共存 | |
| C. | 铁片放入过量的稀硝酸中:3Fe+8H++2NO${\;}_{3}^{-}$═3Fe2++2NO↑+4H2O | |
| D. | 氯化铝溶液中加入过量氨水反应实质是Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ |
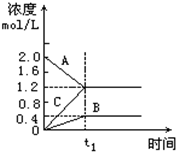 如图表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间,t1为2分钟.试回答:
如图表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间,t1为2分钟.试回答: