6.FeS2的结构类似于Na2O2,是一种过硫化物,与酸反应时首先生成H2S2,H2S2类似于H2O2,易分解:H2S2═H2S+S↓.实验室制取H2S时,某学生误将FeS2当作了FeS反应完后,不可能生成的物质为( )
| A. | H2S | B. | S | C. | Fe2+ | D. | Fe3+ |
5.通过实验观察,某气体有下列性质:①有刺激性气味,②可使品红溶液褪色,③溶于水,溶液能使蓝色石蕊试纸变红,④通入浓硝酸中,无红棕色气体产生,据此,该气体可能是( )
| A. | HCl | B. | Cl2 | C. | SO2 | D. | NH3 |
4.某有机物M的结构简式如下: 下列有关M的叙述中正确的是( )
下列有关M的叙述中正确的是( )
 下列有关M的叙述中正确的是( )
下列有关M的叙述中正确的是( )| A. | M的分子式为:C12H15O5N2 | |
| B. | M可以发生水解反应、中和反应、加成反应、消去反应 | |
| C. | M的水解产物中一定含有醇类 | |
| D. | 1 molM最多可以与1L4mol/L的NaOH溶液完全反应 |
3.合成氨是人类科学技术上的一项重大突破.工业上以天然气为原料合成氨.其生产工艺如下:造气阶段→转化阶段→分离净化→合成阶段
(1)造气阶段的反应为:CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.1kJ/mol
①在一密闭容器中进行上述反应,测得 CH4的物质的量浓度随反应时间的变化如图1所示.反应中处于平衡状态的时间为5min-10min、12min后;10min时,改变的外界条件可能是升高温度.
②如图2所示,在初始容积相等的甲、乙两容器中分别充入等物质的量的CH4和H2O.在相同温度下发生反应,并维持反应过程中温度不变.则达到平衡时,两容器中CH4的转化率大小关系为:α甲(CH4)<α乙(CH4);

(2)转化阶段发生的可逆反应为:CO(g)+H2O(g)?CO2(g)+H2(g),一定温度下,反应的平衡常数为K=1.某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
此时反应中正、逆反应速率的关系式是a(填序号).
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
(3)合成氨反应为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol?1
①依据温度对合成氨反应的影响,在如图3坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图.
②根据勒夏特列原理,简述提高合成氨原料转化率的一种方法增大压强或降低温度或分离液氨.
(1)造气阶段的反应为:CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.1kJ/mol
①在一密闭容器中进行上述反应,测得 CH4的物质的量浓度随反应时间的变化如图1所示.反应中处于平衡状态的时间为5min-10min、12min后;10min时,改变的外界条件可能是升高温度.
②如图2所示,在初始容积相等的甲、乙两容器中分别充入等物质的量的CH4和H2O.在相同温度下发生反应,并维持反应过程中温度不变.则达到平衡时,两容器中CH4的转化率大小关系为:α甲(CH4)<α乙(CH4);

(2)转化阶段发生的可逆反应为:CO(g)+H2O(g)?CO2(g)+H2(g),一定温度下,反应的平衡常数为K=1.某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
(3)合成氨反应为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol?1
①依据温度对合成氨反应的影响,在如图3坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图.
②根据勒夏特列原理,简述提高合成氨原料转化率的一种方法增大压强或降低温度或分离液氨.
2.工业精炼铜的如图所示(如图),下列有关说法正确的是( )
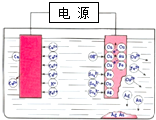

| A. | 右边电极材料为精铜 | |
| B. | 电解质溶液可选择CuSO4溶液 | |
| C. | 随着电解的进行,溶液中Cu2+浓度逐渐增加 | |
| D. | 阳极质量的减小量等于阴极质量的增加量 |
1.目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位.镍能形成多种不同的化合物.图1是镍的一种配合物的结构,图2是一种镍的氧合物的晶胞.判断下列说法正确的是( )


| A. | 图2可能表示的是氧化镍(NiO)的晶胞 | |
| B. | 图1中C、N、O的第一电离能C>N>O | |
| C. | 图2中离镍原子最近的镍原子数共为8个 | |
| D. | 图1分子中存在的化学键有共价键、配位键、氢键 |
20. 在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是
在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是
( )
 在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是
在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )
| A. | 200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol•L-1•min-1 | |
| B. | 由图乙可知,反应xA(g)+yB(g)?zC(g)的△H<0,且a=2 | |
| C. | 若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数减小.达到平衡时,A的体积分数小于0.5 | |
| D. | 200℃时,起始向容器中充入0.2 mol A、0.4 mol B和0.4 mol C,反应达到平衡前的速率:v(正)<v(逆) |
19.等物质的量的氯化钡、硫酸钾和AgNO3溶于水形成混合溶液,用石墨电极电解此溶液,一段时间后,阴、阳两极产生的气体的体积比为3:2.下列说法正确的是( )
| A. | 两极共生成三种气体 | |
| B. | 阴极反应式为:Ag++e-═Ag | |
| C. | 阳极始终发生“2Cl--2e-═Cl2↑”的反应 | |
| D. | 向电解后的溶液中通入适量的HCl气体可使溶液复原到电解前的状态 |
17.元素的性质呈现周期性变化的根本原因是满( )
0 171829 171837 171843 171847 171853 171855 171859 171865 171867 171873 171879 171883 171885 171889 171895 171897 171903 171907 171909 171913 171915 171919 171921 171923 171924 171925 171927 171928 171929 171931 171933 171937 171939 171943 171945 171949 171955 171957 171963 171967 171969 171973 171979 171985 171987 171993 171997 171999 172005 172009 172015 172023 203614
| A. | 元素的相对原子质量递增,量变引起质变 | |
| B. | 元素原子核外电子排布呈周期性变化 | |
| C. | 元素的原子半径由大到小变化 | |
| D. | 元素的化合价呈周期性变化 |
