题目内容
2.工业精炼铜的如图所示(如图),下列有关说法正确的是( )
| A. | 右边电极材料为精铜 | |
| B. | 电解质溶液可选择CuSO4溶液 | |
| C. | 随着电解的进行,溶液中Cu2+浓度逐渐增加 | |
| D. | 阳极质量的减小量等于阴极质量的增加量 |
分析 A.电解精炼粗铜时,粗铜作阳极、纯铜作阴极;
B.根据离子放电顺序,硫酸根离子在电解法精炼铜时不放电;
C.电解精炼铜溶液中铜离子浓度减少;
D.阳极除铜溶解,还有其它金属溶解,所以质量的减小量不等于阴极质量的增加量.
解答 解:A.电解精炼铜时,粗铜作阳极,该电极上Zn、Fe、Ni、Cu失电子溶解,精铜作阴极,该极上是铜离子得电子,右边电极材料铜溶解,所以该电极为阳极为粗铜,故A错误;
B.电解法精炼铜时,阳极主要是粗铜溶解,阴极是铜离子得电子析出,电解质溶液选择CuSO4溶液时,硫酸根离子不参与放电,电解质溶液可选择CuSO4溶液,故B正确;
C.电解精炼铜时,粗铜做阳极含有铁、锌、镍等活泼金属,精铜做阴极,电解过程中电子守恒,溶液中的铜离子浓度减少,故C错误;
D.电解精炼铜时,粗铜做阳极含有铁、锌、镍等活泼金属溶解,阴极是铜离子得电子析出,所以质量的减小量不等于阴极质量的增加量,故D错误;
故选B.
点评 本题考查了电解原理,明确电解时阴阳极上得失电子及离子放电顺序是解本题关键,易错选项是D,注意粗铜做阳极含有铁、锌、镍等活泼金属溶解,为易错点,题目难度中等.

练习册系列答案
相关题目
4.下列物质中属于电解质的是( )
①汞②液氨③氯化钠④盐酸⑤干冰⑥蔗糖⑦氯化银.
①汞②液氨③氯化钠④盐酸⑤干冰⑥蔗糖⑦氯化银.
| A. | ①③④ | B. | ③⑦ | C. | ②③④ | D. | ⑤⑥ |
10.下列实验或反应中,最后固体质量增加的是( )
| A. | 铜丝在空气中灼烧后迅速伸入乙醇蒸气中 | |
| B. | 铁粉与硫粉物质的量之比为1:1时混合加热 | |
| C. | 锌粉加入到氯化铜溶液中 | |
| D. | 去除氧化膜的铝条插入到浓硝酸中 |
17.元素的性质呈现周期性变化的根本原因是满( )
| A. | 元素的相对原子质量递增,量变引起质变 | |
| B. | 元素原子核外电子排布呈周期性变化 | |
| C. | 元素的原子半径由大到小变化 | |
| D. | 元素的化合价呈周期性变化 |
7.取10g氢气和CH3OH的混合物在氧气中完全燃烧,将其产物和足量的过氧化钠反应,反应后固体的质量增加了( )
| A. | 9 g | B. | 10 g | C. | 11 g | D. | 12 g |
14.科学家研究表明:聚乙炔经溴或碘掺杂之后导电性会提高到金属水平,如今聚乙炔已用于制备太阳能电池、半导体材料和电活性聚合物等.下列有关聚乙炔的叙述错误的是( )
| A. | 聚乙炔属于混合物 | B. | 聚乙炔的分子中不含有碳碳叁键 | ||
| C. | 聚乙炔的相对分子质量为26 | D. | 聚乙炔中碳的质量分数为92.3% |
11.下列说法正确的是 ( )
| A. | 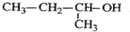 的命名为:2-甲基-1-丙醇 的命名为:2-甲基-1-丙醇 | |
| B. | 有机物 (俗称“一滴香”)的一种含苯环的同分异构体能发生银镜反应 (俗称“一滴香”)的一种含苯环的同分异构体能发生银镜反应 | |
| C. | 布洛芬结构如图所示 该物质可发生氧化、还原、加成、消去、取代反应 该物质可发生氧化、还原、加成、消去、取代反应 | |
| D. | 经测定乙二醇和苯组成的混合物中氧的质量分数为8%,则此混合物中碳的质量分数是84% |
12.对于0.1mol•L-1Na2SO3溶液,正确的是( )
| A. | 升高温度,溶液的pH降低 | |
| B. | 加入少量NaOH固体,c(SO32- )与c(Na+)均增大 | |
| C. | c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-) | |
| D. | c(Na+)=2c(SO32-)+c(HSO3-)+c(H2SO3) |