题目内容
20. 在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是
在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )
| A. | 200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol•L-1•min-1 | |
| B. | 由图乙可知,反应xA(g)+yB(g)?zC(g)的△H<0,且a=2 | |
| C. | 若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数减小.达到平衡时,A的体积分数小于0.5 | |
| D. | 200℃时,起始向容器中充入0.2 mol A、0.4 mol B和0.4 mol C,反应达到平衡前的速率:v(正)<v(逆) |
分析 A.由图Ⅰ可知,200℃时平衡时,B的物质的量变化量为0.4mol-0.2mol=0.2mol,根据v=$\frac{\frac{△n}{V}}{△t}$计算v(B);
B.由图Ⅱ可知,n(A):n(B)一定时,温度越高平衡时C的体积分数越大,说明升高温度平衡向正反应移动,据此判断反应热效应;在一定的温度下只要A、B起始物质的量之比刚好等于平衡化学方程式化学计量数之比,平衡时生成物C的体积分数就最大,由图Ⅰ判断200℃时A、B的起始物质的量,据此计算a的值;
C.温度和平衡常数之间有关,绝热下,随着反应进行,温度降低,根据温度对平衡移动的影响知识来回答;
D、200℃时,向容器中充入2 mol A 和1 mol B达到平衡等效为原平衡增大压强,根据图Ⅰ中A、B、C的物质的量变化量之比等于化学计量数之比确定x、y、z,计算浓度商与化学平衡常数大小,判断化学平衡移动方向,得到答案.
解答 解:A.由图Ⅰ可知,200℃时5min达到平衡,平衡时B的物质的量变化量为0.4mol-0.2mol=0.2mol,故v(B)=$\frac{\frac{0.2mol}{2L}}{5min}$=0.02 mol•L-1•min-1,故A错误;
B.由图Ⅱ可知,n(A):n(B)一定时,温度越高平衡时C的体积分数越大,说明升高温度平衡向正反应移动,升高温度平衡向吸热反应移动,故正反应为吸热反应,即△H>0;图Ⅰ可知,200℃时平衡时,A的物质的量变化量为0.8mol-0.4mol=0.4mol,B的物质的量变化量为0.2mol,在一定的温度下只要A、B起始物质的量之比刚好等于平衡化学方程式化学计量数之比,平衡时生成物C的体积分数就最大,A、B的起始物质的量之比=0.4mol:0.2mol=2,即a=2,故B错误;
C、反应是吸热反应,若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,随着反应进行,温度降低,所以化学平衡常数减小,平衡时在逆向进行的基础上建立的,所以达到平衡时,A的体积分数大于0.5,故C错误;
D、由图Ⅰ可知,200℃时平衡时,A、B、C的物质的量变化量分别为0.4mol、0.2mol、0.2mol,物质的量之比等于化学计量数之比,故x:y:z=0.4mol:0.2mol:0.2mol=2:1:1,平衡时A、B、C浓度分别为:0.2mol/L、0.1mol/L、0.1mol/L,化学平衡常数K=$\frac{0.1}{0.{2}^{2}×0.1}$=25,加入0.2 mol A、0.4 mol B和0.4 mol C,浓度商为:$\frac{0.2}{0.{1}^{2}×0.2}$=100>25,化学平衡向逆反应方向移动,故v(正)<v(逆),故D正确;
故选D.
点评 本题考查化学平衡图象、反应速率计算、影响化学平衡的因素、化学平衡有关计算等,难度中等,注意C选项中理解稀有气体对化学平衡移动的影响.

| A. | 向沸水中滴加饱和氯化铁溶液可制取氢氧化铁胶体 | |
| B. | 可见光透过氢氧化铁胶体时,发生丁达尔现象 | |
| C. | 氢氧化铁胶体放置一段时间后会产生沉淀 | |
| D. | 氢氧化铁胶粒的大小在1-100nm之间 |
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀的pH | 1.9 | 7.0 | 4.7 |
| 完全沉淀的pH | 3.2 | a | 6.7 |
(1)化学上通常认为残留在溶液中的离子浓度小于1×10-5mol/L时,沉淀就达到完全.已知Fe(OH)2的Ksp约为1.0×10-15,则a=9.
(2)加入氧化剂的目的是将Fe2+氧化成Fe3+,X应选择C.
A.K2Cr2O7 B.浓HNO3 C.H2O2 D.KMnO4
(3)加入的物质Y是CuO[Cu(OH)2、CuCO3、Cu2(OH)2CO3也可以].
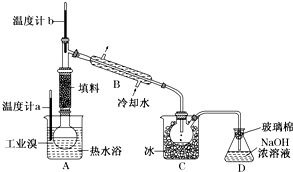
(4)设计实验从溶液Ⅲ中获得纯净的CuCl2•2H2O.简要描述实验步骤应在HCl气流中加热蒸发结晶,过滤、冰水洗涤、低温烘干.
| A. | HCl | B. | Cl2 | C. | SO2 | D. | NH3 |
| A. | 乙烯的比例模型: | B. | 丙烷分子的球棍模型: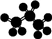 | ||
| C. | 醋酸钠的分子式:CH3COONa | D. | 乙酸的结构简式:CH3COOH |
| A. | “辽宁舰”上用于舰载机降落拦阻索的是一种特种钢缆,属于新型无机非金属材料 | |
| B. | 新型氢动力计程车的投入使用有益于减少雾霾的产生 | |
| C. | 新型复合材料使手机、电脑等电子产品更轻巧、实用和新潮 | |
| D. | 生物柴油是由动植物油脂与甲醇或乙醇,在酸或碱的催化及高温下进行反应,或在温和的条件下,用酶催化反应,生成的高级脂肪酸甲酯或乙酯 |
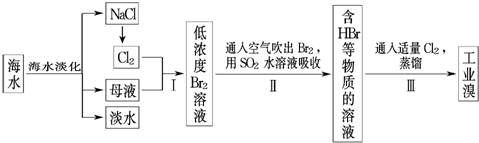
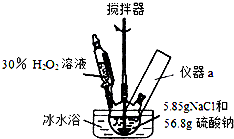 4Na2SO4•2H2O2•NaCl又称固体双氧水,具有漂白、杀菌、消毒作用,又由于其稳定性比过碳酸钠(2Na2CO3•3H2O2)固体更好,因而具有广泛的应用前景.某小组合成该固体双氧水的实验步骤和装置示意图如下:
4Na2SO4•2H2O2•NaCl又称固体双氧水,具有漂白、杀菌、消毒作用,又由于其稳定性比过碳酸钠(2Na2CO3•3H2O2)固体更好,因而具有广泛的应用前景.某小组合成该固体双氧水的实验步骤和装置示意图如下:Ⅰ.合成:往三颈瓶中加入56.8g硫酸钠和5.85gNaCl的固体混合物,开启搅拌器;将稍过量的(约70mL)30%H2O2溶液在20~30min内逐滴分批加入.并控制反应温度15~35℃,加完料后持续搅拌15min,反应结束后过滤,低温干燥得到产品.
Ⅱ.产品稳定性分析:取Ⅰ中所得产品置于干燥器内保存一个月,并分别在放置前、放置后取一定质量的样品溶于水,加适量稀硫酸酸化,用0.1000mol/L酸性高锰酸钾滴定,测定产品中双氧水的含量,以此分析产品的稳定性.所得实验数据如表
数据 时间 | 样品取用数量(g) | 平均V(KMnO4)/mL |
| 放置前测定 | a | 25.00 |
| 放置一个月后测定 | a | 24.90 |
b.产品稳定性=(放置一个月后双氧水的质量分数/放置前双氧水的质量分数)×100%
请回答下列问题:
(1)装置图里方框中应添加仪器a,其名称为温度计;写出合成4Na2SO4•2H2O2•NaCl的化学方程式:4Na2SO4+2H2O2+NaCl=4Na2SO4•2H2O2•NaCl.
(2)该合成反应过程中,关键是控制温度,其合理的措施是:ACD
A.逐滴滴加H2O2 B.选用Na2SO4和NaCl固体,而不用其饱和溶液
C.不断搅拌 D.冰水浴
(3)该合成反应过程中30%的H2O2溶液不应大大过量的原因减小产品的溶解损失,提高产率.
(4)4Na2SO4•2H2O2•NaCl固体比过碳酸钠(2Na2CO3•3H2O2)固体更稳定的可能原因是_2Na2CO3•3H2O2中碳酸钠水解呈碱性,而双氧水在碱性条件容易分解.
(5)产品分析实验时,高锰酸钾溶液装于滴定管中,当滴定到达终点时的现象是溶液从无色刚好变为浅红色,且保持30s不褪色.
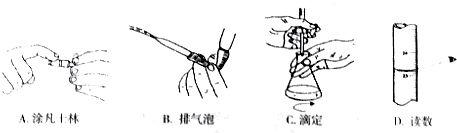
下列关于该滴定实验过程中的仪器选择和操作都正确的是AC
(6)该产品的“产品稳定性”=99.6%.