4.室温下,下列各组离子能大量共存的是( )
| A. | 稀硫酸中:K+、Mg2+、AlO2-、NO3- | |
| B. | Na2S溶液中:SO42-、K+、Cl-、Cu2+ | |
| C. | $\frac{Kw}{c({H}^{+})}$=10-13 mol•L-1溶液中:Fe3+、NH4+、Mg2+、SO42- | |
| D. | 通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3- |
3.下列解释实验现象的反应方程式正确的是( )
| A. | 双氧水中加入稀硫酸和KI溶液:H2O2+2I-+2H+═I2+2H2O | |
| B. | 电解氯化镁溶液产生黄绿色气体:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 将切开的金属Na露置在空气中,表面由光亮逐渐变暗:2Na+O2═Na2O2 | |
| D. | 向Ca(HCO3)2溶液中加入过量的烧碱溶液,出现白色沉淀:HCO3-+Ca2++OH-═CaCO3↓+H2O |
18. 乙醇脱水反应在不同温度条件下得到的产物组成不同.表是常压、某催化剂存在条件下,分别以等量乙醇在不同温度下进行脱水实验获得的数据,每次实验反应时间均相同.
乙醇脱水反应在不同温度条件下得到的产物组成不同.表是常压、某催化剂存在条件下,分别以等量乙醇在不同温度下进行脱水实验获得的数据,每次实验反应时间均相同.
已知:乙醇和乙醚(CH3CH2OCH2CH3)的沸点分别为78.4℃和34.5℃.请回答下列问题:
(1)乙醇脱水制乙烯的反应是吸热(填“放热”、“吸热”)反应,若增大压强,平衡逆向(选填“正向”、“逆向”、“不”)移动;
(2)已知:150℃时,1mol乙醇蒸汽脱水转变为1mol乙烯,反应热的数值为46KJ,写出该反应的热化学方程式C2H5OH(g)→C2H4(g)+H2O(g)△H=+46KJ/mol;
(3)写出乙醇脱水制乙醚的反应的平衡常数表达式K=$\frac{[C{\;}_{2}H{\;}_{5}OC{\;}_{2}H{\;}_{5}]•[H{\;}_{2}O]}{[C{\;}_{2}H{\;}_{5}OH]{\;}^{2}}$.当乙醇起始浓度相同时,平衡常数K值越大,表明ab(填字母).
a.乙醇的转化率越高 b.反应进行得越完全
c.达到平衡时乙醇的浓度越大 d.化学反应速率越快
(4)根据表中数据分析,150℃时乙醇催化脱水制取的乙醚产量大于(选填“大于”、“小于”、“等于”)125℃时;为了又快又多地得到产品,乙醇制乙醚合适的反应温度区域是150~175℃.
0 171382 171390 171396 171400 171406 171408 171412 171418 171420 171426 171432 171436 171438 171442 171448 171450 171456 171460 171462 171466 171468 171472 171474 171476 171477 171478 171480 171481 171482 171484 171486 171490 171492 171496 171498 171502 171508 171510 171516 171520 171522 171526 171532 171538 171540 171546 171550 171552 171558 171562 171568 171576 203614
 乙醇脱水反应在不同温度条件下得到的产物组成不同.表是常压、某催化剂存在条件下,分别以等量乙醇在不同温度下进行脱水实验获得的数据,每次实验反应时间均相同.
乙醇脱水反应在不同温度条件下得到的产物组成不同.表是常压、某催化剂存在条件下,分别以等量乙醇在不同温度下进行脱水实验获得的数据,每次实验反应时间均相同.| 温度(℃) | 乙醇转化率(%) | 有机产物含量(体积分数) | |
| 乙烯(%) | 乙醚(%) | ||
| 125 | 20 | 8.7 | 90.2 |
| 150 | 68 | 16.7 | 82.2 |
| 175 | 88 | 32.3 | 66.8 |
| 200 | 90 | 86.9 | 12.1 |
(1)乙醇脱水制乙烯的反应是吸热(填“放热”、“吸热”)反应,若增大压强,平衡逆向(选填“正向”、“逆向”、“不”)移动;
(2)已知:150℃时,1mol乙醇蒸汽脱水转变为1mol乙烯,反应热的数值为46KJ,写出该反应的热化学方程式C2H5OH(g)→C2H4(g)+H2O(g)△H=+46KJ/mol;
(3)写出乙醇脱水制乙醚的反应的平衡常数表达式K=$\frac{[C{\;}_{2}H{\;}_{5}OC{\;}_{2}H{\;}_{5}]•[H{\;}_{2}O]}{[C{\;}_{2}H{\;}_{5}OH]{\;}^{2}}$.当乙醇起始浓度相同时,平衡常数K值越大,表明ab(填字母).
a.乙醇的转化率越高 b.反应进行得越完全
c.达到平衡时乙醇的浓度越大 d.化学反应速率越快
(4)根据表中数据分析,150℃时乙醇催化脱水制取的乙醚产量大于(选填“大于”、“小于”、“等于”)125℃时;为了又快又多地得到产品,乙醇制乙醚合适的反应温度区域是150~175℃.
 纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数.图中:①空气 ②某溶液 ③纯碱 ④某溶液 ⑤碱石灰
纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数.图中:①空气 ②某溶液 ③纯碱 ④某溶液 ⑤碱石灰 ;装置C的作用是吸收生成的二氧化碳气体中的水蒸气;如果撤去装置C,则会导致测定结果偏高(填“偏大”、“偏小”或“不变”)
;装置C的作用是吸收生成的二氧化碳气体中的水蒸气;如果撤去装置C,则会导致测定结果偏高(填“偏大”、“偏小”或“不变”) A~F都是中学化学常见物质,它们间的相互转化关系如图所示,其中A、D、F是化合物,E是非金属单质.
A~F都是中学化学常见物质,它们间的相互转化关系如图所示,其中A、D、F是化合物,E是非金属单质. .
.
 B
B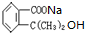
 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ +nH2O;反应类型:缩聚反应
+nH2O;反应类型:缩聚反应 +H2O;反应类型:消去反应
+H2O;反应类型:消去反应 ;反应类型:加聚反应.
;反应类型:加聚反应.