题目内容
1.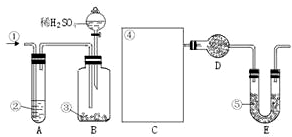 纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数.图中:①空气 ②某溶液 ③纯碱 ④某溶液 ⑤碱石灰
纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数.图中:①空气 ②某溶液 ③纯碱 ④某溶液 ⑤碱石灰其实验步骤是:
a.按图所示,组装好实验仪器,并检查其气密性.
b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g).
c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内.
d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“①”处缓慢鼓入空气,直到B容器中不再产生气体为止.
e.准确称量干燥管D的总质量(设为m2 g).
根据上述实验回答下列问题:
(1)该实验进行到操作d时,要缓缓鼓入空气,其作用是将装置中的CO2全部赶入D中.装置A中盛装的液体“②”应选用NaOH溶液,装置A的作用是吸收空气中的CO2,如果撤去装置A,直接向B中缓缓鼓入空气,则会导致实验测定结果(填“偏大”“偏小”或“不变”)偏大.
(2)在空白格内画出装置C及试剂④是
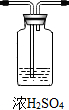 ;装置C的作用是吸收生成的二氧化碳气体中的水蒸气;如果撤去装置C,则会导致测定结果偏高(填“偏大”、“偏小”或“不变”)
;装置C的作用是吸收生成的二氧化碳气体中的水蒸气;如果撤去装置C,则会导致测定结果偏高(填“偏大”、“偏小”或“不变”)(3)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为$\frac{2650(m{\;}_{2}-m{\;}_{1})}{11n}$%(用m1、m2、n表示).
(4)装置E的作用是防止空气中的水汽和CO2进入D被吸收.
分析 (1)从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,把生成的二氧化碳全部赶入装置D中;A中是氢氧化钠溶液吸收空气中的二氧化碳气体;如果撤去装置A,空气中的二氧化碳可能被碱石灰吸收,根据二氧化碳计算碳酸钠的质量就会变大,据此判断;
(2)装置C中是浓硫酸吸收生成的二氧化碳气体中的水蒸气,若撤销装置C会导致干燥管中质量增大,测定结果偏高;
(3)干燥管质量变化为生成二氧化碳的质量,结合元素守恒计算碳酸钠的质量分数;
(4)装置E是为了防止空气中的水蒸气和二氧化碳进入装置D造成测定误差.
解答 解:(1)从“1”处缓慢鼓入空气,使纯碱和H2SO4反应产生的CO2全部排出,把生成的二氧化碳全部赶入装置D中;A中是氢氧化钠溶液,用来吸收空气中的二氧化碳气体,如果撤去装置A,空气中的二氧化碳可能被碱石灰吸收,根据二氧化碳计算碳酸钠的质量就会变大,所以会导致实验测定结果偏大,
故答案为:将装置中的CO2全部赶入D中;NaOH溶液;吸收空气中的CO2;偏大;
(2)装置C中是浓硫酸吸收生成的二氧化碳气体中的水蒸气,需要用洗气瓶,装置为: 若撤销装置C会导致干燥管中质量增大,测定结果偏高;
若撤销装置C会导致干燥管中质量增大,测定结果偏高;
故答案为: ;吸收生成的二氧化碳气体中的水蒸气;偏高;
;吸收生成的二氧化碳气体中的水蒸气;偏高;
(3)干燥管质量变化为生成二氧化碳的质量,为(m2-m1)g结合元素守恒计算碳酸钠的质量分数=$\frac{\frac{{m}_{2}-m{\;}_{1}}{44}×106}{n}$×100%=$\frac{2650(m{\;}_{2}-m{\;}_{1})}{11n}$%;
故答案为:$\frac{2650(m{\;}_{2}-m{\;}_{1})}{11n}$%;
(4)装置E是为了防止空气中的水蒸气和二氧化碳进入装置D造成测定误差;
故答案为:防止空气中的水汽和CO2进入D被吸收.
点评 本题考查了物质组成的实验探究和过程分析判断,主要是气体除杂的理解应用,元素守恒计算分析,掌握基础是关键,题目难度中等.

 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案| A. | b、a、d、c、e | B. | e、b、a、d、c | C. | b、a、e、d、c | D. | c、d、e、a、b |
| A. | 乙醇是一种无色无味的液体,可以与水以任意比例互溶 | |
| B. | 1mol乙醇中含有共价键的数目是7NA(NA表示阿伏伽德罗常数的值) | |
| C. | 乙醇与乙二醇、丙三醇互为同系物 | |
| D. | 乙醇可以直接被氧化为乙酸 |
【提出问题】久置“双吸剂”的成分是什么?
【做出猜想】久置“双吸剂”中可能有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究1】取固体样品研磨,用磁铁吸引,磁铁上沾有黑色粉末,说明“双吸剂”中一定有Fe.再用磁铁反复吸引后,残留固体用于后续探究活动.
【实验探究2】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量探究实验1的残留固体放入试管中,加入蒸馏水 | 试管外壁不发烫 | 固体中一定没有 |
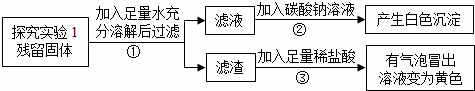
【实验结论】步骤②产生白色沉淀,说明久置的“双吸剂”中含有Ca(OH)2,其反应的化学方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
步骤③有气泡冒出,溶液变为黄色,说明久置的“双吸剂”中含有Fe2O3和CaCO3.
| A. | 上述物质都有发生了氧化还原反应 | |
| B. | 过氧化钠在反应中转移了2 mol电子 | |
| C. | 质量增加的情况是①>③>④>② | |
| D. | 质量增加的情况是②>①>③>① |
| A. | 含1molFeCl3的饱和溶液最多可形成胶体粒子数为NA | |
| B. | 4.6gNa与稀盐酸反应,转移电子数一定为0.2NA | |
| C. | 10.6gNa2CO3晶体中含CO32-数目为0.1NA | |
| D. | 常温下,22gCO2含碳氧双键数目为NA |
| A. | 金刚石和石墨物理性质不同,是因为它们的碳原子排列方式不同 | |
| B. | 一氧化碳、二氧化碳、葡萄糖都属于有机物 | |
| C. | 木炭、一氧化碳在一定条件下都能与氧化铜反应 | |
| D. | 大气中二氧化碳的消耗途径主要是绿色植物的光合作用 |