13.下列离子方程式正确的是( )
| A. | 铜粉溶于FeCl3溶液的离子方程式:Cu+Fe3+=Cu2++Fe2+ | |
| B. | 将Na2O2固体投入H218O中:2H218O+2Na2O2═4OH-+4Na++18O2↑ | |
| C. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓ | |
| D. | Ca(HCO3)2溶液与足量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
10.铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝同主族元素,元素符号是Tl,以下对铊的性质的推析不正确的是( )
| A. | 铊是易导电的银白色金属 | B. | 能生成+3价离子 | ||
| C. | 氢氧化铊是两性氢氧化物 | D. | Tl3+的氧化能力比Al3+弱 |
9.下列各组中的化学性质比较,不正确的是( )
①酸性:HClO4>HBrO4>HIO4
②还原性:I-<Cl-<F-
③碱性:NaOH>Mg(OH)2>Al(OH)3
④稳定性:PH3>H2S>HCl
⑤半径:S2->Na+>Mg2+>O2-
⑥氧化性:Li+>Na+>K+>Rb+>Cs+.
①酸性:HClO4>HBrO4>HIO4
②还原性:I-<Cl-<F-
③碱性:NaOH>Mg(OH)2>Al(OH)3
④稳定性:PH3>H2S>HCl
⑤半径:S2->Na+>Mg2+>O2-
⑥氧化性:Li+>Na+>K+>Rb+>Cs+.
| A. | ①②④ | B. | ②④⑤ | C. | ①⑤⑥ | D. | ②③⑤ |
8.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 5.6g铁粉与足量Cl2反应,失去的电子数为0.2NA | |
| B. | 1.8g重水(D2O)中含有的质子数和电子数均为1.0NA | |
| C. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA | |
| D. | 常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
5. 在密闭容器中进行下列反应:M(气)+N(气)?R(气)+2A此反应符合下面图象,(纵坐标为R的质量百分含量)下列叙述正确的是( )
在密闭容器中进行下列反应:M(气)+N(气)?R(气)+2A此反应符合下面图象,(纵坐标为R的质量百分含量)下列叙述正确的是( )
0 170623 170631 170637 170641 170647 170649 170653 170659 170661 170667 170673 170677 170679 170683 170689 170691 170697 170701 170703 170707 170709 170713 170715 170717 170718 170719 170721 170722 170723 170725 170727 170731 170733 170737 170739 170743 170749 170751 170757 170761 170763 170767 170773 170779 170781 170787 170791 170793 170799 170803 170809 170817 203614
 在密闭容器中进行下列反应:M(气)+N(气)?R(气)+2A此反应符合下面图象,(纵坐标为R的质量百分含量)下列叙述正确的是( )
在密闭容器中进行下列反应:M(气)+N(气)?R(气)+2A此反应符合下面图象,(纵坐标为R的质量百分含量)下列叙述正确的是( )| A. | 正反应吸热,A是气体 | B. | 正反应吸热,A是固体 | ||
| C. | 正反应放热,A是气体 | D. | 正反应放热,A是固体或液体 |
 ;
; .
.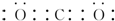
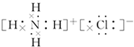

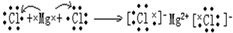 .
.
 A、B、C为短周期元素,在周期表中所处位置如图所示,A、C两种元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处位置如图所示,A、C两种元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.