题目内容
4. A、B、C为短周期元素,在周期表中所处位置如图所示,A、C两种元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处位置如图所示,A、C两种元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.(1)写出A、B、C三种元素的名称:氮、硫、氟.
(2)A位于元素周期表中第二周期,第ⅤA族.
(3)B、C两元素的氢化物的稳定性为HF>NH3(填分子式)
(4)将过量的A的气态氢化物与B的最高价氧化物对应水化物反应的产物为(NH4)2SO4.(填化学式)
分析 A、B、C为短周期元素,根据元素在周期表中位置知,A和C位于第二周期、B位于第三周期,设B原子序数为x,则A原子序数为x-9、C原子序数为x-7,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等,则x-9+x-7=x,则x=16,所以B是S元素,则A是N元素、C是F元素,再结合原子结构分析解答.
解答 解:A、B、C为短周期元素,根据元素在周期表中位置知,A和C位于第二周期、B位于第三周期,设B原子序数为x,则A原子序数为x-9、C原子序数为x-7,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等,则x-9+x-7=x,则x=16,所以B是S元素,则A是N元素、C是F元素,
(1)通过以上分析知,A、B、C分别是氮、硫、氟元素,故答案为:氮;硫;氟;
(2)A是N元素,N原子核外有2个电子层、最外层电子数是5,所以N元素位于第二周期第VA族,故答案为:二;ⅤA;
(3)B、C两元素分别是N、F元素,非金属性越强氢化物越稳定,所以稳定性:HF>NH3,故答案为:HF;NH3;
(4)A为N元素,对应的氢化物为氨气,B对应的最高价氧化物的水化物为硫酸,过量的氨气与硫酸反应的方程式为:2NH3+H2SO4═(NH4)2SO4,故答案为:(NH4)2SO4.
点评 本题考查位置结构性质关系的综合应用,为高频考点,题目难度不大,注意根据质子数关系结合元素所在周期表中的位置推断元素的种类.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列说法中正确的是( )
| A. | FeCl3 溶液和Fe(OH)3 胶体外观均是透明液体. | |
| B. | 制备Fe(OH)3 胶体的方法是将饱和FeCl3 溶液加热煮沸 | |
| C. | 28gCO和C2H4混合气体含有的分子数为2NA | |
| D. | 溶液和胶体的本质区别是丁达尔效应 |
15.在体积为1L的两个恒容密闭容器中,分别充入1molCO和1molH2O(g)的混合气体,进行如下化学反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
(1)1100℃时,前10min该反应的化学反应速率v(CO2)=0.025mol/(L.min).
(2)计算1100℃时该反应的化学平衡常数K=$\frac{4}{9}$.
(3)能判断该反应是否达到化学平衡状态的依据是bc.
(a)容器中压强不变
(b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O)
(d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡向右移动(选填“向右”或“向左”或“不”),再达到平衡时,H2百分含量不变(选填“增大”或“减小”或“不变”).
| 0min | 10min | 20min | 30min | 40min | 50min | |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
(2)计算1100℃时该反应的化学平衡常数K=$\frac{4}{9}$.
(3)能判断该反应是否达到化学平衡状态的依据是bc.
(a)容器中压强不变
(b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O)
(d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡向右移动(选填“向右”或“向左”或“不”),再达到平衡时,H2百分含量不变(选填“增大”或“减小”或“不变”).
12.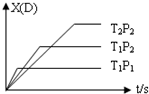 已知可逆反应 mA(g)+nB(g)?pC(g)+qD(g),反应中D的物质的量分数X(D)与时间t的关系如图,则下列叙述正确的是( )
已知可逆反应 mA(g)+nB(g)?pC(g)+qD(g),反应中D的物质的量分数X(D)与时间t的关系如图,则下列叙述正确的是( )
 已知可逆反应 mA(g)+nB(g)?pC(g)+qD(g),反应中D的物质的量分数X(D)与时间t的关系如图,则下列叙述正确的是( )
已知可逆反应 mA(g)+nB(g)?pC(g)+qD(g),反应中D的物质的量分数X(D)与时间t的关系如图,则下列叙述正确的是( )| A. | 正反应为放热反应 | B. | m+n>p+q | ||
| C. | T1<T2 | D. | P1<P2 |
9.下列各组中的化学性质比较,不正确的是( )
①酸性:HClO4>HBrO4>HIO4
②还原性:I-<Cl-<F-
③碱性:NaOH>Mg(OH)2>Al(OH)3
④稳定性:PH3>H2S>HCl
⑤半径:S2->Na+>Mg2+>O2-
⑥氧化性:Li+>Na+>K+>Rb+>Cs+.
①酸性:HClO4>HBrO4>HIO4
②还原性:I-<Cl-<F-
③碱性:NaOH>Mg(OH)2>Al(OH)3
④稳定性:PH3>H2S>HCl
⑤半径:S2->Na+>Mg2+>O2-
⑥氧化性:Li+>Na+>K+>Rb+>Cs+.
| A. | ①②④ | B. | ②④⑤ | C. | ①⑤⑥ | D. | ②③⑤ |
16.根据陈述的知识,类推得出的结论正确的是( )
| A. | 镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O | |
| B. | 乙烯(CH2=CH2)可使酸性高锰酸钾溶液褪色,则丙烯(CH3-CH=CH2)也可以使其褪色 | |
| C. | CO2和SiO2化学式相似,则CO2与SiO2的物理性质也相似 | |
| D. | 金刚石的硬度大,则C60的硬度也大 |
 与
与
 与
与
 与
与
 与
与
