题目内容
11.(1)请用下列10种物质的序号填空:①O2 ②H2 ③NH4NO3 ④K2O2 ⑤NaOH ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2只由非金属元素组成的离子化合物是③;既有离子键又有极性键的是③⑤.
(2)写出下列物质的电子式:
①CO2
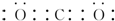
②NH4Cl
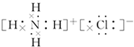
(3)用电子式表示下列物质的形成过程
①H2O

②MgCl2
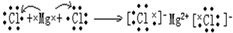 .
.
分析 (1)一般来说,活泼金属和活泼非金属所以之间易形成离子键,不同非金属元素之间易形成极性键,同种非金属元素之间易形成非极性键;
(2)二氧化碳分子中每个O原子和C原子之间形成两对共用电子对;
氯化铵是离子化合物,氯离子和铵根离子之间存在离子键、N-H原子之间存在极性键;
(3)H、O原子通过共用电子对形成共价化合物;Mg、Cl原子之间通过得失电子形成离子化合物.
解答 解:(1)一般来说,活泼金属和活泼非金属所以之间易形成离子键,不同非金属元素之间易形成极性键,同种非金属元素之间易形成非极性键,只有非金属元素组成的离子化合物是硝酸铵,既有离子键又有极性键的是硝酸铵、氢氧化钠,故答案为:③;③⑤;
(2)①二氧化碳分子中每个O原子和C原子之间形成两对共用电子对,电子式为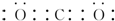 ,故答案为:
,故答案为: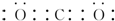 ;
;
②氯化铵是离子化合物,氯离子和铵根离子之间存在离子键、N-H原子之间存在极性键,电子式为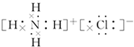 ,故答案为:
,故答案为: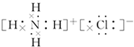 ;
;
(3)H、O原子通过共用电子对形成共价化合物,其形成过程为 ;Mg、Cl原子之间通过得失电子形成离子化合物,其形成过程为
;Mg、Cl原子之间通过得失电子形成离子化合物,其形成过程为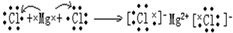 ,
,
故答案为: ;
;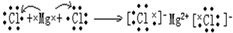 .
.
点评 本题考查离子化合物判断、化合物形成过程等知识点,为高频考点,明确离子化合物、共价化合物区别及化合物形成过程是解本题关键,难点是电子式的书写,题目难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
11.下列仪器或装置在使用前需要检查气密性的是( )
| A. | 容量瓶 | B. | 蒸馏烧瓶 | C. | 分液漏斗 | D. | 酸(碱)式滴定管 |
16.根据陈述的知识,类推得出的结论正确的是( )
| A. | 镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O | |
| B. | 乙烯(CH2=CH2)可使酸性高锰酸钾溶液褪色,则丙烯(CH3-CH=CH2)也可以使其褪色 | |
| C. | CO2和SiO2化学式相似,则CO2与SiO2的物理性质也相似 | |
| D. | 金刚石的硬度大,则C60的硬度也大 |
3.已知C5H11Br有8种同分异构体,则C6H12O属于醛的结构有( )
| A. | 16种 | B. | 11种 | C. | 8种 | D. | 6种 |
20.下列有关元素非金属性的比较,正确的是( )
| A. | 进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱 | |
| B. | HCl溶液的酸性比H2S溶液的酸性强,则氯元素的非金属性比硫强 | |
| C. | H2O的沸点高于H2S,则氧元素的非金属性强于硫元素 | |
| D. | 浓H2SO4的氧化性强于HClO4,可确定硫和氯两种元素的非金属性强弱 |
1.下列说法不正确的是( )
| A. | 实验室少量的金属钠保存在煤油或石蜡油里 | |
| B. | 金属钠着火,用干燥的沙土来灭火 | |
| C. | 铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物 | |
| D. | 铁制炊具不宜用来煎炒食物,因为铁要与水反应 |
 与
与
 与
与
 与
与
 与
与