11.铋(Bi)在医药方面有重要应用.${\;}_{83}^{209}$Bi与${\;}_{83}^{210}$Bi的关系是( )
| A. | 同一种核素 | B. | 互为同分异构体 | C. | 互为同素异形体 | D. | 互为同位素 |
8.下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,按要求回答下列问题.
(1)元素①~⑨中,金属性最强的元素是Na(填元素符号).
(2)元素③的原子结构示意图是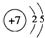 .
.
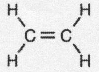
(3)元素①和②可以形成多种化合物,其中是天然气主要成分的化合物的电子式是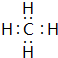 ,该化合物的二氯代物有1种.
,该化合物的二氯代物有1种.
(4)元素⑦、⑧、⑨的最高价氧化物对应的水化物的酸性由强到弱的顺序是HClO4>H2SO4>H2SiO3(填化学式).
(5)下列可以判断元素④和⑨非金属性强弱的是bc(填序号).
a.单质的熔点④比⑨低 b.单质与氢气反应④比⑨剧烈
c.气态氢化物稳定性④比⑨强 d.单质的密度④比⑨小
(6)元素⑥的单质和元素⑤的最高价氧化物对应的水化物的溶液反应,其化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
| 族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)元素③的原子结构示意图是
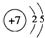 .
.(3)元素①和②可以形成多种化合物,其中是天然气主要成分的化合物的电子式是
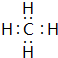 ,该化合物的二氯代物有1种.
,该化合物的二氯代物有1种.(4)元素⑦、⑧、⑨的最高价氧化物对应的水化物的酸性由强到弱的顺序是HClO4>H2SO4>H2SiO3(填化学式).
(5)下列可以判断元素④和⑨非金属性强弱的是bc(填序号).
a.单质的熔点④比⑨低 b.单质与氢气反应④比⑨剧烈
c.气态氢化物稳定性④比⑨强 d.单质的密度④比⑨小
(6)元素⑥的单质和元素⑤的最高价氧化物对应的水化物的溶液反应,其化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
5.下列冶炼金属的原理不正确的是( )
| A. | 电解饱和食盐水制备金属钠 | B. | 加热分解Ag2O制备金属银 | ||
| C. | Fe2O3与CO高温下反应制备金属铁 | D. | Cu2S与O2高温下反应制备金属铜 |
4.将CO2转化成有机物可有效地实现碳循环.原子利用率为目标产物的总质量与全部反应物的总质量之比,则以下反应中理论上原子利用率最高的是( )
| A. | CO2+CH4$→_{△}^{催化剂}$CH3COOH | |
| B. | 2CO2+6H2$→_{△}^{催化剂}$C2H5OH十3H2O | |
| C. | 2CO2+6H2$→_{△}^{催化剂}$CH2=CH2+4H2O | |
| D. | 6CO2+6H2O$\stackrel{光照/叶绿素}{→}$C6H12O6+6O2 |
3.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 食盐水和糖水 | B. | 泥沙和水 | C. | 碘和四氯化碳 | D. | 水和四氯化碳 |
2.元素周期表中某区域的一些元素多用于制造半导体材料,它们是( )
0 169950 169958 169964 169968 169974 169976 169980 169986 169988 169994 170000 170004 170006 170010 170016 170018 170024 170028 170030 170034 170036 170040 170042 170044 170045 170046 170048 170049 170050 170052 170054 170058 170060 170064 170066 170070 170076 170078 170084 170088 170090 170094 170100 170106 170108 170114 170118 170120 170126 170130 170136 170144 203614
| A. | 金属元素和非金属元素分界线附近的元素 | |
| B. | 右上方区域的非金属元素 | |
| C. | 过渡元素 | |
| D. | 稀有气体元素 |
 .
.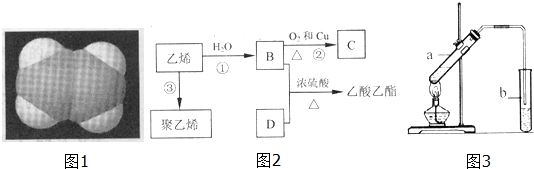
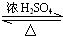 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.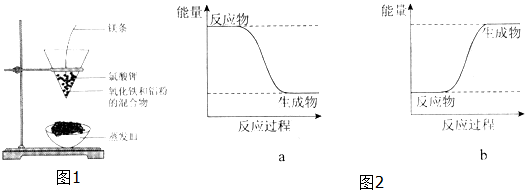
 Al2O3+2 Fe,其能量变化可用图2中的a(填“a”或“b”)表示.
Al2O3+2 Fe,其能量变化可用图2中的a(填“a”或“b”)表示.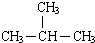 );
);