9.下列叙述不正确的是( )
| A. | 因为氯气具有酸性,所以可与烧碱或石灰乳反应制备含氯消毒剂 | |
| B. | 除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液 | |
| C. | 过氧化钠中含有离子键和非极性共价键,阴离子与阳离子的物质的量之比为1:2 | |
| D. | 植物油的不饱和程度高于动物油,植物油更易氧化变质 |
8.化学与生产、生活、社会密切相关,下列说法不正确的是( )
| A. | 只要符合限量,“食用色素”、“亚硝酸盐”可以作为某些食品的添加剂 | |
| B. | 发泡塑料饭盒主要材质是高分子材料,不适于盛放含油较多的食品 | |
| C. | 蛋白质、淀粉、纤维素、油脂等都能在人体内水解并提供能量 | |
| D. | 纯净的二氧化硅是现代光学及光纤制品的基本原料 |
5.如图图示与对应的叙述相符的是( )


| A. | 图甲表示反应:4CO(g)+2NO2(g)?N2(g)+4CO2(g)△H<0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2 | |
| B. | 图乙表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(g)的影响,乙的压强比甲的压强大 | |
| C. | 图丙表示的反应是吸热反应,该图表明催化剂能改变化学反应的焓变 | |
| D. | 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)?N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 |
4.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 一定条件下6.4g SO2与足量氧气反应生成SO3,转移电子数为0.2 NA | |
| B. | 1 mol AlCl3在熔融状态时离子总数为0.4NA | |
| C. | 标况下,11.2 L氯气完全溶于1 L水中,所得溶液中Cl-和ClO-两种粒子数之和为NA | |
| D. | 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2 NA |
3.下列各组离子在指定分散系中一定能大量共存的是( )
| A. | 明矾溶液中:Na+、Mg2+、NO3-、HCO3- | |
| B. | 澄清透明的溶液中:Na+、K+、MnO4-、ClO- | |
| C. | pH=0的溶液中:Al3+、Ag(NH3)2+、Cl-、SO42- | |
| D. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、SO32- |
2.关于下列说法错误的是( )
| A. | 乙醇、乙二醇、丙三醇互为同系物;H2、D2、T2互为同素异形体 | |
| B. | 绿矾、碱石灰、苏打、干冰分别属于纯净物、混合物、电解质、非电解质 | |
| C. | 乙烯水化、铁铝钝化、植物油氢化、纯碱晶体风化等过程中都包含化学变化 | |
| D. | 蛋白质、纤维素、硝化纤维等都是高分子化合物 |
1.解释下列实验事实的离子方程式中,不准确的是( )
0 168594 168602 168608 168612 168618 168620 168624 168630 168632 168638 168644 168648 168650 168654 168660 168662 168668 168672 168674 168678 168680 168684 168686 168688 168689 168690 168692 168693 168694 168696 168698 168702 168704 168708 168710 168714 168720 168722 168728 168732 168734 168738 168744 168750 168752 168758 168762 168764 168770 168774 168780 168788 203614
| A. | 在Na2SO4溶液中滴入Ba(OH)2溶液,产生白色沉淀:Ba2++SO42-=BaSO4↓ | |
| B. | 向H2O中加入少量Na2O2,产生无色气体:2Na2O2+2H2O=O2↑+4OH-+4Na+ | |
| C. | 向Cl2水中滴入适量Fe(NO3)2 溶液,溶液变为黄色:2Fe2++Cl2=2Fe3++2Cl- | |
| D. | 向淀粉KI溶液中滴加酸性H2O2溶液,溶液变蓝色:H2O2+2I-+2H+=I2+2H2O |
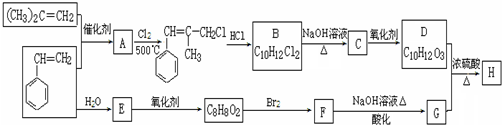
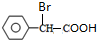 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$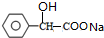 +NaBr+H2O.
+NaBr+H2O.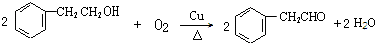 .
.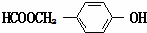 (写结构简式).
(写结构简式).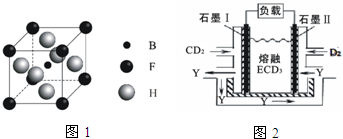 有A、B、C、D、E、F、G、H八种原子序数依次增大的元素(原子序数均小于30).A原子的核外电子数与电子层数相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,A、E同主族,F的基态原子s能级的电子总数与p能级的电子数相等,B、G同族,H的基态原子的3d轨道电子数是4s电子数的4倍.请回答下列问题:
有A、B、C、D、E、F、G、H八种原子序数依次增大的元素(原子序数均小于30).A原子的核外电子数与电子层数相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,A、E同主族,F的基态原子s能级的电子总数与p能级的电子数相等,B、G同族,H的基态原子的3d轨道电子数是4s电子数的4倍.请回答下列问题:
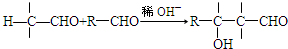

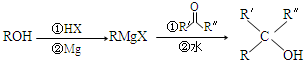
 .X与苯酚生成高聚物反应的化学方程式
.X与苯酚生成高聚物反应的化学方程式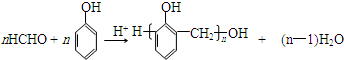 .
.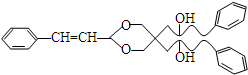 .
. .
.