题目内容
20.X是常温下的气态醛,A比X的相对分子质量大14,Y是最简单的芳香醛.现用X、Y、A制备有机物H,其合成路线如图:
已知:①
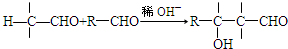
②

③
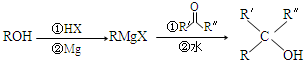
完成下列有关问题:
(1)X的名称:甲醛.
(2)C+D→G的化学方程式:
 .X与苯酚生成高聚物反应的化学方程式
.X与苯酚生成高聚物反应的化学方程式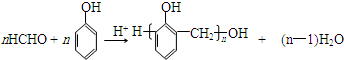 .
.(3)H的结构简式是:
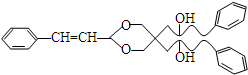 .
.(4)C能发生的反应是ad.
a.取代反应 b.皂化反应 c.消去反应 d.置换反应 e.还原反应 f.加聚反应
(5)符合下列条件的C的同分异构体有3种
①属于直链化合物 ②与C具有相同的官能团 ③每个碳原子上最多只有一个官能团
(6)X与Y反应的生成物有多种同分异构体,写出能使FeCl3溶液呈紫色,且其核磁共振谱上有五组峰,峰面积之比为1:2:2:2:1.则该同分异构体与新制Cu(OH)2反应的方程式为
 .
.
分析 X是常温下的气态醛,应为甲醛,A比X的相对分子质量大14,由题给信息可知应为CH3CHO,Y是最简单的芳香醛,为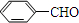 ,C由B和氢气发生加成反应,可知B应含有4个O原子,则B由CH3CHO和3个HCHO发生反应生成,B为
,C由B和氢气发生加成反应,可知B应含有4个O原子,则B由CH3CHO和3个HCHO发生反应生成,B为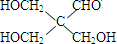 ,C为
,C为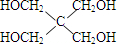 ,由D的分子式结合提给信息可知D含有苯环、醛基和碳碳双键,应为
,由D的分子式结合提给信息可知D含有苯环、醛基和碳碳双键,应为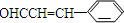 ,E为
,E为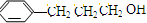 ,F为
,F为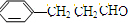 ,由信息②可知G为
,由信息②可知G为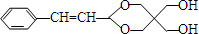 ,由信息③可知H为
,由信息③可知H为 ,以此解答该题.
,以此解答该题.
解答 解:X是常温下的气态醛,应为甲醛,A比X的相对分子质量大14,由题给信息可知应为CH3CHO,Y是最简单的芳香醛,为 ,C由B和氢气发生加成反应,可知B应含有4个O原子,则B由CH3CHO和3个HCHO发生反应生成,B为
,C由B和氢气发生加成反应,可知B应含有4个O原子,则B由CH3CHO和3个HCHO发生反应生成,B为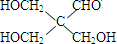 ,C为
,C为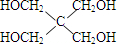 ,由D的分子式结合提给信息可知D含有苯环、醛基和碳碳双键,应为
,由D的分子式结合提给信息可知D含有苯环、醛基和碳碳双键,应为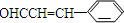 ,E为
,E为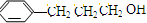 ,F为
,F为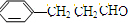 ,由信息②可知G为
,由信息②可知G为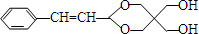 ,由信息③可知H为
,由信息③可知H为 ,
,
(1)由以上分析可知X为甲醛,故答案为:甲醛;
(2)C为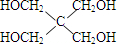 ,D为
,D为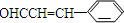 ,二者反应的方程式为
,二者反应的方程式为 ,甲醛与苯酚发生缩聚反应生成酚醛树脂,反应的方程式为
,甲醛与苯酚发生缩聚反应生成酚醛树脂,反应的方程式为 ,
,
故答案为: ;
; ;
;
(3)由以上分析可知H为 ,故答案为:
,故答案为: ;
;
(4)C为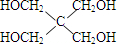 ,含有羟基,可发生取代反应,可与活泼金属发生置换反应生成氢气,不能发生其它反应,
,含有羟基,可发生取代反应,可与活泼金属发生置换反应生成氢气,不能发生其它反应,
故答案为:ad;
(5)C为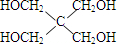 ,对应的同分异构体中,①属于直链化合物 ②与C具有相同的官能团 ③每个碳原子上最多只有一个官能团,可有CH2OHCHOHCHOHCHOHCH3、CH2OHCHOHCH2CHOHCH2OH、CH2OHCH2CHOHCHOHCH2OH,共3种,
,对应的同分异构体中,①属于直链化合物 ②与C具有相同的官能团 ③每个碳原子上最多只有一个官能团,可有CH2OHCHOHCHOHCHOHCH3、CH2OHCHOHCH2CHOHCH2OH、CH2OHCH2CHOHCHOHCH2OH,共3种,
故答案为:3;
(6)X与Y反应的生成物有多种同分异构体,写出能使FeCl3溶液呈紫色,且其核磁共振谱上有五组峰,峰面积之比为1:2:2:2:1,为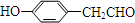 ,含有醛基,可在加热条件下与新制备氢氧化铜浊液发生氧化还原反应,方程式为
,含有醛基,可在加热条件下与新制备氢氧化铜浊液发生氧化还原反应,方程式为 ,
,
故答案为: .
.
点评 本题考查有机物的推断,为高考常见题型,侧重于学生的分析能力的考查,注意把握题给信息,为解答该题的关键,答题时可根据官能团的性质以及题给信息用正推的方法,难度中等.

 习题精选系列答案
习题精选系列答案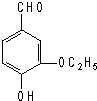
| A. | 1 mol乙基香草醛最多可与1 mol氢气发生加成反应 | |
| B. | 乙基香草醛可与Br2的CCl4溶液发生加成反应 | |
| C. | 1mol乙基香草醛可与含3 mol NaOH的水溶液完全反应 | |
| D. | 乙基香草醛能被酸性高锰酸钾、银氨溶液、新制的氢氧化铜等氧化 |
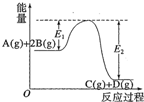
| A. | Q=E2 | |
| B. | 在反应体系中加入催化剂,反应速率增大,E1减小,E2不变 | |
| C. | Q>0,仅升高温度,当反应再次达到平衡时,A的平衡浓度增大 | |
| D. | 1molA(g)和2molB(g)充分反应后放热QkJ |
| A. | 对于Si+O2═SiO2,每当新形成2NA个Si-O键,需要断开NA个Si-Si键 | |
| B. | 12.0g熔融的NaHSO4中含有的阳离子数为0.1NA | |
| C. | 次氯酸光照分解产生22.4mL气体(标准状况)转移的电子数为0.002NA | |
| D. | 电解精炼铜时,若阴极析出32g铜,则转移的电子数为NA |

| A. | 图甲表示反应:4CO(g)+2NO2(g)?N2(g)+4CO2(g)△H<0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2 | |
| B. | 图乙表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(g)的影响,乙的压强比甲的压强大 | |
| C. | 图丙表示的反应是吸热反应,该图表明催化剂能改变化学反应的焓变 | |
| D. | 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)?N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 |
| A. | 糖类物质的分子都可以用Cm(H2O)n来表示 | |
| B. | 凡能溶于水具有甜味的物质都属于糖类 | |
| C. | 糖类都能发生水解反应 | |
| D. | 糖类是多羟基醛或多羟基酮以及水解能生成它们的化合物 |

 I、离子液体是一种室温熔融盐,为非水体系,由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体作电解液时,可在钢制品上电镀铝.
I、离子液体是一种室温熔融盐,为非水体系,由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体作电解液时,可在钢制品上电镀铝.