15.酚酞是中学阶段常用的酸碱指示剂,结构简式如图所示:下列关于酚酞的说法错误的是( )
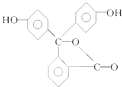

| A. | 酚酞与水可以形成氢键 | |
| B. | 酚酞的分子式为C20H14O4 | |
| C. | 酚酞结构中含有羟基(-OH),故酚酞属于醇 | |
| D. | 酚酞在一定条件下能够发生加成反应 |
14.下列实验不能成功的是( )
| A. | 将电石和水反应后的气体通入溴水中,如果溴水褪色,证明乙炔和溴发生了反应 | |
| B. | 实验室制溴苯时,将苯与液溴混合后加到有铁丝的反应容器中 | |
| C. | 往酸性KMnO4溶液中通入乙烯来证明乙烯有还原性 | |
| D. | 乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
11.将2.4g镁和铝的混合物粉末溶于75mL 4mol/L的盐酸中,反应一段时间后,再加入250mL 1.5mol/L的NaOH溶液后待反应完全,此时溶液中大量存在的是( )
| A. | Na+、Mg2+ | B. | Na+、Al3+、Mg2+ | C. | Na+、Mg2+、[Al(OH)4]- | D. | Na+、[Al(OH)4]- |
10.A、B、C、D四种非金属元素,A、B在反应中各结合1个电子形成稳定结构,放出能量B<A;氢化物稳定性HD>HA;原子序数C<B,其稳定结构的核外电子数相等.则四种元素非金属性由强到弱的顺序正确的是( )
| A. | A、B、C、D | B. | B、A、C、D | C. | D、A、B、C | D. | B、A、D、C |
9.将甲、乙两种金属的性质相比较,
已知:①甲与H2O反应比乙与H2O反应剧烈;
②甲单质能从乙的盐溶液中置换出单质乙;
③甲的最高价氧化物对应水化物的碱性比乙的最高价氧化物对应水化物的碱性强;
④与非金属单质反应时,甲原子失电子数目比乙原子失电子数目多;
⑤甲单质的熔、沸点比乙的低.
能说明甲的金属性比乙强的是( )
已知:①甲与H2O反应比乙与H2O反应剧烈;
②甲单质能从乙的盐溶液中置换出单质乙;
③甲的最高价氧化物对应水化物的碱性比乙的最高价氧化物对应水化物的碱性强;
④与非金属单质反应时,甲原子失电子数目比乙原子失电子数目多;
⑤甲单质的熔、沸点比乙的低.
能说明甲的金属性比乙强的是( )
| A. | ①④ | B. | ①②③ | C. | ③⑤ | D. | ①②③④⑤ |
8.下列比较错误的是( )
| A. | 金属性:Na>Mg>Al | B. | 非金属性:Cl>S>P>Si | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 酸性:HClO>H2SO3>H3PO4>H4SiO4 |
7.下列关于元素周期表和元素周期律的说法中正确的是( )
| A. | 在周期表中,元素的族序数都等于其原子的最外层电子数 | |
| B. | 周期表中非金属性最强的元素,其最高价氧化物的水化物酸性也最强 | |
| C. | 同主族元素随原子核电荷数的递增,原子半径依次减小 | |
| D. | 第ⅦA族元素的单质,随分子量的增大,熔、沸点逐渐升高 |
6.对于化学方程式SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑,有关叙述正确的是( )
0 167050 167058 167064 167068 167074 167076 167080 167086 167088 167094 167100 167104 167106 167110 167116 167118 167124 167128 167130 167134 167136 167140 167142 167144 167145 167146 167148 167149 167150 167152 167154 167158 167160 167164 167166 167170 167176 167178 167184 167188 167190 167194 167200 167206 167208 167214 167218 167220 167226 167230 167236 167244 203614
| A. | 反应中SiO2是氧化剂,C是还原剂 | |
| B. | 硅元素被还原了,碳元素被氧化了 | |
| C. | 在反应中C既是氧化剂又是还原剂 | |
| D. | 在反应中氧化剂与还原剂的物质的量之比为1:1 |
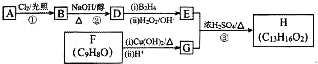

 ;
;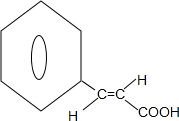 +(CH3)2CHCH2OH$?_{△}^{浓硫酸}$H2O+
+(CH3)2CHCH2OH$?_{△}^{浓硫酸}$H2O+ ;
;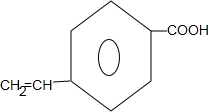 .
. ,A与B在原子的电子层结构上的相同点是最外层均有4个电子.
,A与B在原子的电子层结构上的相同点是最外层均有4个电子.