题目内容
9.将甲、乙两种金属的性质相比较,已知:①甲与H2O反应比乙与H2O反应剧烈;
②甲单质能从乙的盐溶液中置换出单质乙;
③甲的最高价氧化物对应水化物的碱性比乙的最高价氧化物对应水化物的碱性强;
④与非金属单质反应时,甲原子失电子数目比乙原子失电子数目多;
⑤甲单质的熔、沸点比乙的低.
能说明甲的金属性比乙强的是( )
| A. | ①④ | B. | ①②③ | C. | ③⑤ | D. | ①②③④⑤ |
分析 元素的金属性越强,其最高价氧化物的水化物碱性越强,与水或酸置换出氢气越容易,较活泼金属能置换出较不活泼金属,据此分析解答.
解答 解:①元素的金属性越强,其与水反应越剧烈,甲与H2O反应比乙与H2O反应剧烈,说明甲的金属性活动性大于乙,故正确;
②较活泼金属能置换出较不活泼金属,甲单质能从乙的盐溶液中置换出单质乙,说明甲的还原性大于乙,则金属甲大于乙,故正确;
③元素的金属性越强,其最高价氧化物的水化物碱性越强,甲的最高价氧化物对应水化物的碱性比乙的最高价氧化物对应水化物的碱性强,说明甲的金属性大于乙,故正确;
④金属性强弱与失电子难易程度有关,与失电子多少无关,故错误;
⑤金属性强弱与失电子难易程度有关,与单质的熔、沸点无关,故错误;
故选B.
点评 本题考查元素金属性强弱判断,为高考高频点,明确金属性强弱与金属失电子难易程度有关,与失电子多少无关,为易错点,熟练掌握金属性、非金属性强弱判断方法.

练习册系列答案
相关题目
19.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,5.6L四氯化碳含有的分子数为0.25NA | |
| B. | 2.8g[CH2 CH2]n 中含有的碳原子数为0.2NA | |
| C. | 1mol苯分子中含有C=C双键数为3NA | |
| D. | 乙烷和丙烯的物质的量共1mol,完全燃烧生成水分子数为3NA |
20.下列实验过程中产生的现象与对应的图象不相符合的是( )
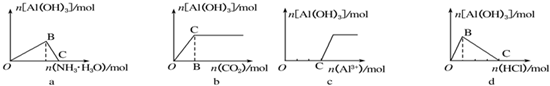
①在AlCl3溶液中滴加氨水至过量
②向Na[Al(OH)4]溶液中逐渐通入二氧化碳至过量
③向Na[Al(OH)4]溶液中滴加稀盐酸至过量边滴边振荡
④向NaOH溶液中滴加AlCl3溶液至过量边滴边振荡.

①在AlCl3溶液中滴加氨水至过量
②向Na[Al(OH)4]溶液中逐渐通入二氧化碳至过量
③向Na[Al(OH)4]溶液中滴加稀盐酸至过量边滴边振荡
④向NaOH溶液中滴加AlCl3溶液至过量边滴边振荡.
| A. | a① | B. | b② | C. | c④ | D. | d③ |
14.下列实验不能成功的是( )
| A. | 将电石和水反应后的气体通入溴水中,如果溴水褪色,证明乙炔和溴发生了反应 | |
| B. | 实验室制溴苯时,将苯与液溴混合后加到有铁丝的反应容器中 | |
| C. | 往酸性KMnO4溶液中通入乙烯来证明乙烯有还原性 | |
| D. | 乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
1.萘( )是最简单的稠环芳香烃.下列关于萘的说法中正确的是( )
)是最简单的稠环芳香烃.下列关于萘的说法中正确的是( )
 )是最简单的稠环芳香烃.下列关于萘的说法中正确的是( )
)是最简单的稠环芳香烃.下列关于萘的说法中正确的是( )| A. | 萘与足量氢气充分加成的产物一氯代物有2种 | |
| B. | 1mol萘最多可与6mol H2加成 | |
| C. | 萘的一氯代物有2种,二氯代物有10种 | |
| D. | 萘属于苯的同系物 |
19.实验测得BeCl2为共价化合物,两个Be-Cl键间的夹角应为( )
| A. | 60° | B. | 90° | C. | 120° | D. | 180° |
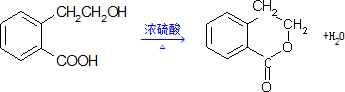 .
. .
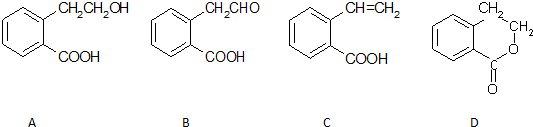
.
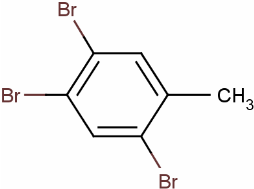 +3HBr.
+3HBr.