11. 常温下,用0.1000mol/L 的盐酸滴定0.1000mol/L Na2CO3溶液25.00mL.用pH传感器测得混合溶液的pH变化曲线如图.下列说法正确的是( )
常温下,用0.1000mol/L 的盐酸滴定0.1000mol/L Na2CO3溶液25.00mL.用pH传感器测得混合溶液的pH变化曲线如图.下列说法正确的是( )
 常温下,用0.1000mol/L 的盐酸滴定0.1000mol/L Na2CO3溶液25.00mL.用pH传感器测得混合溶液的pH变化曲线如图.下列说法正确的是( )
常温下,用0.1000mol/L 的盐酸滴定0.1000mol/L Na2CO3溶液25.00mL.用pH传感器测得混合溶液的pH变化曲线如图.下列说法正确的是( )| A. | c→d发生的主要离子反应:HCO3-+H+═H2O+CO2 | |
| B. | 在b点 时,c(HCO3-)>c(CO32-)>c(OH-) | |
| C. | 在d点 时,c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) | |
| D. | 在e点 时完全反应后溶液中水电离出c(H+)=1.0×10-7mol•L-1 |
10. 以熔融CaF2-CaO作电解质,用下图所示袋置获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )
以熔融CaF2-CaO作电解质,用下图所示袋置获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )
 以熔融CaF2-CaO作电解质,用下图所示袋置获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )
以熔融CaF2-CaO作电解质,用下图所示袋置获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )| A. | 整套装置工作前后中CaO的总量基本不变 | |
| B. | 阳极的电极反应式为2Ca2++4e-=2Ca | |
| C. | 石墨电极作阳极,质量不变 | |
| D. | 电解过程中,F-和O2-向阴极移动 |
9. 加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示.先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解.下列说法正确的是( )
加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示.先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解.下列说法正确的是( )
 加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示.先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解.下列说法正确的是( )
加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示.先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解.下列说法正确的是( )| A. | b电极是负极 | |
| B. | 装置中的离子交换膜是阳离子交换膜 | |
| C. | 阳极电极反应:4OH--4e-═2H2O+O2↑ | |
| D. | a极区的KI最终转变为KIO3 |
8. 连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol•L-1的NaOH溶液滴定10mL0.01mol•L-1 H2N2O2溶液,溶液pH随加入NaOH溶液体积的变化如图所示,下列有关说法中正确的是( )
连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol•L-1的NaOH溶液滴定10mL0.01mol•L-1 H2N2O2溶液,溶液pH随加入NaOH溶液体积的变化如图所示,下列有关说法中正确的是( )
 连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol•L-1的NaOH溶液滴定10mL0.01mol•L-1 H2N2O2溶液,溶液pH随加入NaOH溶液体积的变化如图所示,下列有关说法中正确的是( )
连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol•L-1的NaOH溶液滴定10mL0.01mol•L-1 H2N2O2溶液,溶液pH随加入NaOH溶液体积的变化如图所示,下列有关说法中正确的是( )| A. | H2N2O2在水溶液中的电离方程式为H2N2O2═2H++N2O22- | |
| B. | 该滴定过程应该选择甲基橙作为指示剂 | |
| C. | a点的溶液中:c(Na+)+c(H+)═c(OH-)+c(N2O22-)+c(H N2O2-) | |
| D. | b点的溶液中:c(Na+)>c(H N2O2-)>c(OH-)>c(H2N2O2)>c(N2O22-) |
7. 电镀产生的工业废水含有的重金属离子(Cu2+、Ni2+等)和CN形成难以除去的络合物,用电解法制备高铁酸钠(Na2FeO4)处理废水是目前比较先进的方法.已知氰化氢有毒易挥发.电解装置如图所示,下列选项正确的是( )
电镀产生的工业废水含有的重金属离子(Cu2+、Ni2+等)和CN形成难以除去的络合物,用电解法制备高铁酸钠(Na2FeO4)处理废水是目前比较先进的方法.已知氰化氢有毒易挥发.电解装置如图所示,下列选项正确的是( )
 电镀产生的工业废水含有的重金属离子(Cu2+、Ni2+等)和CN形成难以除去的络合物,用电解法制备高铁酸钠(Na2FeO4)处理废水是目前比较先进的方法.已知氰化氢有毒易挥发.电解装置如图所示,下列选项正确的是( )
电镀产生的工业废水含有的重金属离子(Cu2+、Ni2+等)和CN形成难以除去的络合物,用电解法制备高铁酸钠(Na2FeO4)处理废水是目前比较先进的方法.已知氰化氢有毒易挥发.电解装置如图所示,下列选项正确的是( )| A. | 铁片连接电源的负极 | |
| B. | 电解时,每生成lmolFeO42-,转移电子3mol | |
| C. | CN被氧化成CO2和N2,Cu2+、Ni2+形成难溶碱而除去 | |
| D. | 已知HFeO4-的氧化性比FeO42-更强,故pH<7时处理废水效率更高 |
4.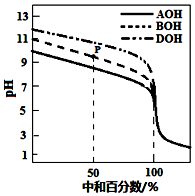 室温下,用相同物质的量浓度的HCl溶液,分别滴定物质的量浓度均为0.1mol•L-1的三种碱(AOH、BOH和DOH)溶液,滴定的曲线如图所示,下列判断正确的是( )
室温下,用相同物质的量浓度的HCl溶液,分别滴定物质的量浓度均为0.1mol•L-1的三种碱(AOH、BOH和DOH)溶液,滴定的曲线如图所示,下列判断正确的是( )
 室温下,用相同物质的量浓度的HCl溶液,分别滴定物质的量浓度均为0.1mol•L-1的三种碱(AOH、BOH和DOH)溶液,滴定的曲线如图所示,下列判断正确的是( )
室温下,用相同物质的量浓度的HCl溶液,分别滴定物质的量浓度均为0.1mol•L-1的三种碱(AOH、BOH和DOH)溶液,滴定的曲线如图所示,下列判断正确的是( )| A. | 滴定时,随着盐酸溶液的滴入,水电离出的c(H+)始终增大 | |
| B. | 滴定至P点时,溶液中:c(Cl-)>c(B+)>c(BOH)>c(OH-)>c(H+) | |
| C. | pH=7时,三种溶液中c(Cl-) 相等 | |
| D. | 当中和百分数达100%时,将三种溶液混合后:c(AOH)+c(BOH)+c(DOH)=c(H+)-c(OH-) |
3.汽车尾气脱硝脱碳主要原理为:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$N2(g)+2CO2(g)+Q(Q>0).
一定条件下密闭容器中,用传感器测得该反应在不同时间NO和CO浓度如表:
完成下列填空:
(1)写出该反应的平衡常数表达式:K=$\frac{c({N}_{2}){c}^{2}(C{O}_{2})}{{c}^{2}(CO){c}^{2}(NO)}$.
(2)前2s内的氮气的平均反应速率是:v(N2)=1.75×10-3mol/(L•s);
达到平衡时,CO的转化率为89%.
(3)业上常采用“低温臭氧氧化脱硫脱硝”技术来同时吸收SO2和氮的氧化物气体(NOx),以获得(NH4)2SO4的稀溶液.在此溶液中,水的电离程度是受到了促进(填“促进”、“抑制”或“没有影响”);
若往(NH4)2SO4溶液中再加入少量稀盐酸,则$\frac{{c(N{H_4}^+)}}{{c(S{O_4}^{2-})}}$值将变大(填“变大”、“变小”或“不变”).
(4)如果向BaCl2溶液中通入足量SO2气体,没有沉淀生成,继续滴加一定量的氨水后,则会生成白色沉淀.用平衡移动原理解释上述现象.饱和SO2溶液中电离产生的SO32-很少,因此没有沉淀,而加入氨水后,促进H2SO3的电离,SO32-离子浓度增大,有沉淀产生.
(5)向另一种可溶性钡盐溶液中通入少量SO2气体,会立即看到白色沉淀,该沉淀的化学式为BaSO4;原可溶性钡盐可能是Ba(NO3)2.
一定条件下密闭容器中,用传感器测得该反应在不同时间NO和CO浓度如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 |
| c(NO)/mol•L-1 | 9.50×10-3 | 4.50×10-3 | 2.50×10-3 | 1.50×10-3 | 1.50×10-3 |
| c(CO)/mol•L-1 | 9.00×10-3 | 4.00×10-3 | 2.00×10-3 | 1.00×10-3 | 1.00×10-3 |
(1)写出该反应的平衡常数表达式:K=$\frac{c({N}_{2}){c}^{2}(C{O}_{2})}{{c}^{2}(CO){c}^{2}(NO)}$.
(2)前2s内的氮气的平均反应速率是:v(N2)=1.75×10-3mol/(L•s);
达到平衡时,CO的转化率为89%.
(3)业上常采用“低温臭氧氧化脱硫脱硝”技术来同时吸收SO2和氮的氧化物气体(NOx),以获得(NH4)2SO4的稀溶液.在此溶液中,水的电离程度是受到了促进(填“促进”、“抑制”或“没有影响”);
若往(NH4)2SO4溶液中再加入少量稀盐酸,则$\frac{{c(N{H_4}^+)}}{{c(S{O_4}^{2-})}}$值将变大(填“变大”、“变小”或“不变”).
(4)如果向BaCl2溶液中通入足量SO2气体,没有沉淀生成,继续滴加一定量的氨水后,则会生成白色沉淀.用平衡移动原理解释上述现象.饱和SO2溶液中电离产生的SO32-很少,因此没有沉淀,而加入氨水后,促进H2SO3的电离,SO32-离子浓度增大,有沉淀产生.
(5)向另一种可溶性钡盐溶液中通入少量SO2气体,会立即看到白色沉淀,该沉淀的化学式为BaSO4;原可溶性钡盐可能是Ba(NO3)2.
2. 常温下,用0.1000mol•L-1的NaOH标准溶液滴定20.00mL0.1000mol•L-1的HCl溶液,滴定曲线如图,下列有关说法正确的是( )
常温下,用0.1000mol•L-1的NaOH标准溶液滴定20.00mL0.1000mol•L-1的HCl溶液,滴定曲线如图,下列有关说法正确的是( )
0 163660 163668 163674 163678 163684 163686 163690 163696 163698 163704 163710 163714 163716 163720 163726 163728 163734 163738 163740 163744 163746 163750 163752 163754 163755 163756 163758 163759 163760 163762 163764 163768 163770 163774 163776 163780 163786 163788 163794 163798 163800 163804 163810 163816 163818 163824 163828 163830 163836 163840 163846 163854 203614
 常温下,用0.1000mol•L-1的NaOH标准溶液滴定20.00mL0.1000mol•L-1的HCl溶液,滴定曲线如图,下列有关说法正确的是( )
常温下,用0.1000mol•L-1的NaOH标准溶液滴定20.00mL0.1000mol•L-1的HCl溶液,滴定曲线如图,下列有关说法正确的是( )| A. | 指示剂变色时,说明反应的酸、碱恰好等物质的量反应 | |
| B. | 当达到滴定终点时才存在c(Na+)+c(H+)=c(Cl-)+c(OH-) | |
| C. | 达到滴定终点时,用甲基橙作指示剂消耗NaOH溶液体积比用酚酞多 | |
| D. | 己知 H+(aq)+OH- (aq)=H2O(l)△H=-57.3 kJ/mol,上述滴定恰好中和时,放出114.6 J的热量 |

 燃煤烟气脱硫有很多方法
燃煤烟气脱硫有很多方法