题目内容
10. 以熔融CaF2-CaO作电解质,用下图所示袋置获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )
以熔融CaF2-CaO作电解质,用下图所示袋置获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )| A. | 整套装置工作前后中CaO的总量基本不变 | |
| B. | 阳极的电极反应式为2Ca2++4e-=2Ca | |
| C. | 石墨电极作阳极,质量不变 | |
| D. | 电解过程中,F-和O2-向阴极移动 |
分析 根据图知,阳极上电极反应式为C+2O2--4e-═CO2↑,阴极上电极反应式为:2Ca2++4e-═2Ca,钙还原二氧化钛反应方程式为:2Ca+TiO2$\frac{\underline{\;一定条件\;}}{.}$Ti+2CaO,“+”接线柱应连接原电池正极,电解过程中,电解质中阳离子向阴极移动、阴离子向阳极移动,据此分析解答.
解答 解:A.阴极上电极反应式为2Ca2++4e-═2Ca,钙还原二氧化钛反应方程式为2Ca+TiO2=Ti+2CaO,在制备金属钛前后,整套装置中CaO的总量不变,故A正确;
B.根据图知,阳极上生成二氧化碳,则阳极反应式为C+2O2--4e-═CO2↑,故B错误;
C.阳极发生反应为C+2O2--4e-═CO2↑,石墨作为阳极,反应需要消耗石墨,则石墨质量会减少,故C错误;
D.电解池中,阴离子向阳极移动,则F-和O2-向阳极移动,故D错误.
故选A.
点评 本题综合考查电解池和原电池知识,为高频考点,侧重于学生的分析能力的考查,注意把握电极方程式的书写,易错选项是A,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.干冰所属晶体类型为( )
| A. | 原子晶体 | B. | 分子晶体 | C. | 金属晶体 | D. | 离子晶体 |
20.Mn和Bi形成的晶体薄膜是一种金属间化合物(晶胞结构如图),有关说法正确的是( )

| A. | 锰价电子排布为3d74s0 | B. | Bi是d区金属 | ||
| C. | 该合金堆积方式是简单立方 | D. | 该晶体的化学式为MnBi |
15.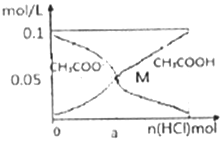 常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )
常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )
 常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )
常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )| A. | 当n(HCl)=1.0×10-3mol时,溶液中 c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-) | |
| B. | M点溶液中水的电离程度比原溶液小 | |
| C. | 随着HCl的通入,c(OH-)/c(CH3COO-) 值不断减小 | |
| D. | 在M 点时,c(H+)-c(OH-)=(a-0.05)mol/L |
2.下列情况会对人体健康造成较大危害的是( )
| A. | 用米醋清洗热水瓶胆内中的水垢(CaCO3) | |
| B. | 家庭生活中常用铁锅煮饭 | |
| C. | 用小苏打(NaHCO3)与发酵面粉混合制糕点 | |
| D. | 用SO2漂白食品 |
19.下列说法错误的是( )
| A. | 分子式相同的,各元素百分含量也相同的物质是同种物质. | |
| B. | 同系物之间具有相似的化学性质. | |
| C. | 乙烯可作香蕉等水果的催熟剂. | |
| D. | 乙烯燃烧时,火焰明亮,同时产生黑烟. |
20.下列反应中,不符合如图所示能量变化的是( )


| A. | 盐酸与NaOH反应 | B. | Na与H2O反应 | ||
| C. | 铝热反应 | D. | NH4Cl与Ba(OH)2•8H2O反应 |

 燃煤烟气脱硫有很多方法
燃煤烟气脱硫有很多方法