1.不同温度下BaCO3在水中的沉淀溶解平衡曲线如图所示(已知T1<T2<T3),下列说法正确的是( )
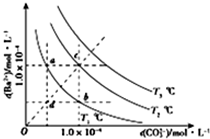

| A. | T2温度下将d点的溶液蒸发浓缩可变为c点 | |
| B. | a点的Ksp小于B点的Ksp | |
| C. | b点溶液中加入BaCl2固体可变为c点 | |
| D. | a点溶液蒸发浓缩恢复到原温度可变为b点 |
2.碲锌镉(Te-Zn-Cd)晶体可以用于制造红外探测器的基础材料,下列有关它的叙述中不正确的是( )
| A. | 它是由Te、Zn、Cd按一定比例混合而成的,无固定的溶沸点 | |
| B. | 它易导电、导热,具有延展性 | |
| C. | 它的熔、沸点比Zn的低 | |
| D. | 它的硬度和强度比Cd的大 |
1.能正确表示下列反应的离子方程式的是( )
| A. | 将铜屑加入 Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+ | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O | |
| C. | 将氯化亚铁酸性溶液和H2O2混合:Fe2++2H++H2O2═Fe3++2H2O | |
| D. | 将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
20.某混合气体中可能含有ClO2、SO2、NO、NO2中的两种或多种.将此无色混合气体通 过品红溶液后,品红溶液褪色;把剩余气体排入空气中,气体很快变为红棕色.下列关于原 混合气体成分的判断正确的是( )
| A. | 肯定没有SO2和NO | B. | 肯定只有NO | ||
| C. | 可能有Cl2和O2 | D. | 肯定没有Cl2、NO2和O2 |
19.下列不能说明氯的非金属性比硫强的事实是( )
①HCl比H2S稳定
②HCl和H2S的水溶液前者的酸性强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl原子能得1个电子变成稳定离子而S原子能得两个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
①HCl比H2S稳定
②HCl和H2S的水溶液前者的酸性强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl原子能得1个电子变成稳定离子而S原子能得两个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
| A. | ②⑤ | B. | ①② | C. | ①②⑤ | D. | ①③⑤ |
18.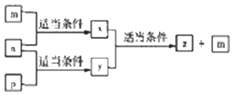 A、B,C、D四种原子序数依次增大的分别位于三个不同短周期的主族元素,m、n、p分别是元素A、C、B、的单质,x、y、z是由A、B、C组成的二元化合物,其中y、z是气体且z是用于配制饮料,它们之间有如下转化关系,D的单质可与热水发生置换反应,下列说法正确的是( )
A、B,C、D四种原子序数依次增大的分别位于三个不同短周期的主族元素,m、n、p分别是元素A、C、B、的单质,x、y、z是由A、B、C组成的二元化合物,其中y、z是气体且z是用于配制饮料,它们之间有如下转化关系,D的单质可与热水发生置换反应,下列说法正确的是( )
 A、B,C、D四种原子序数依次增大的分别位于三个不同短周期的主族元素,m、n、p分别是元素A、C、B、的单质,x、y、z是由A、B、C组成的二元化合物,其中y、z是气体且z是用于配制饮料,它们之间有如下转化关系,D的单质可与热水发生置换反应,下列说法正确的是( )
A、B,C、D四种原子序数依次增大的分别位于三个不同短周期的主族元素,m、n、p分别是元素A、C、B、的单质,x、y、z是由A、B、C组成的二元化合物,其中y、z是气体且z是用于配制饮料,它们之间有如下转化关系,D的单质可与热水发生置换反应,下列说法正确的是( )| A. | D的单质起火燃烧时可用x作灭火剂 | |
| B. | 元素的非金属性:C>A>B | |
| C. | 原了半径:D>C>B>A | |
| D. | B与同族元素的氧化物可发生置换反应,并且做还原剂 |
17. 光能储存一般是指将光能转换为电能或化学能进行储存,利用太阳光、CO2、H2O生成甲醇的光能储存装置如图所示,制备开始时质子交换膜两侧的溶液质量相等.下列叙述不正确的是( )
光能储存一般是指将光能转换为电能或化学能进行储存,利用太阳光、CO2、H2O生成甲醇的光能储存装置如图所示,制备开始时质子交换膜两侧的溶液质量相等.下列叙述不正确的是( )
0 163569 163577 163583 163587 163593 163595 163599 163605 163607 163613 163619 163623 163625 163629 163635 163637 163643 163647 163649 163653 163655 163659 163661 163663 163664 163665 163667 163668 163669 163671 163673 163677 163679 163683 163685 163689 163695 163697 163703 163707 163709 163713 163719 163725 163727 163733 163737 163739 163745 163749 163755 163763 203614
 光能储存一般是指将光能转换为电能或化学能进行储存,利用太阳光、CO2、H2O生成甲醇的光能储存装置如图所示,制备开始时质子交换膜两侧的溶液质量相等.下列叙述不正确的是( )
光能储存一般是指将光能转换为电能或化学能进行储存,利用太阳光、CO2、H2O生成甲醇的光能储存装置如图所示,制备开始时质子交换膜两侧的溶液质量相等.下列叙述不正确的是( )| A. | n型半导体为负极 | |
| B. | X2为O2,H+由b极向a极移动 | |
| C. | b极的电极反应式为CO2+6e-+6H+=CH3OH+H2O | |
| D. | 当制备32g甲醇时,质子交换膜两侧溶液相差104g |