18.${\;}_{53}^{131}$I是常规核裂变产物之一,可以通过测定大气或水中${\;}_{53}^{131}$I的含量变化来检测核电站是否发生泄露,下列有关${\;}_{53}^{131}$I的叙述中不正确的是( )
| A. | ${\;}_{53}^{131}$I的化学性质与${\;}_{53}^{127}$相同 | |
| B. | ${\;}_{53}^{131}$I的原子序数为53 | |
| C. | ${\;}_{53}^{131}$I的核外电子数为78 | |
| D. | ${\;}_{53}^{131}$I原子核内中子数多于质子数 |
17.我国稀土资源丰富,下列有关稀土元素${\;}_{62}^{144}$Sm和${\;}_{62}^{150}$Sm的说法正确的是( )
| A. | ${\;}_{62}^{144}$Sm和${\;}_{62}^{150}$Sm是同一种核素 | |
| B. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm的质量数相同 | |
| C. | ${\;}_{62}^{144}$Sm和${\;}_{62}^{150}$Sm互为同位素 | |
| D. | ${\;}_{62}^{144}$Sm和${\;}_{62}^{150}$Sm的核外电子数和中子数均为62 |
14.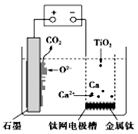 研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金金属钛.下列说法中错误的是
研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金金属钛.下列说法中错误的是
( )
 研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金金属钛.下列说法中错误的是
研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金金属钛.下列说法中错误的是( )
| A. | 阳极的电极反应式为:C+2O2--4e-═CO2↑ | |
| B. | 在制备金属钛前后,整套装置中CaO的总量保持不变 | |
| C. | 若用铅蓄电池作供电电源,“一”接线柱应连接Pb电极 | |
| D. | 由TiO2制得1 mol金属Ti,理论上外电路通过2 mol电子 |
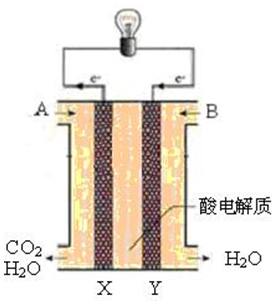
13.如图所示电化学装置中电极均为惰性电极,可用于吸收SO2,阴极排出的溶液可用于吸收NO2,治理环境污染.下列说法正确的是( )


| A. | 其中的离子交换膜需选用阴离子交换膜 | |
| B. | 阴极的电极反应式为:2HSO3-+2e-=S2O42-+2OH- | |
| C. | 阳极的电极反应式为:SO2+2H2O-2e-=SO42-+4H+ | |
| D. | 反应一段时间后将惰性电极换成铁电极,对电极产物不产生影响 |
12.下列说法不正确的是( )
| A. | 麦芽糖及其水解产物均能发生银镜反应 | |
| B. | 用溴水即可鉴别苯酚溶液、2,4-己二烯和甲苯 | |
| C. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| D. | 用甘氨酸( 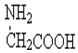 )和丙氨酸( )和丙氨酸( 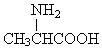 )缩合最多可形成4种二肽(不考虑形成环状) )缩合最多可形成4种二肽(不考虑形成环状) |
10.过量的铁粉与100mL 0.1mol/L的稀盐酸反应,反应速率太快.为了降低此反应速率而不改变产生H2的量,可以使用如下方法中的( )①加H2O ②加NaOH固体 ③滴入过量浓硫酸 ④加少量的NaNO3固体 ⑤加NaCl溶液⑥滴加几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10mL 1mol/L的盐酸.
| A. | ①⑥⑦ | B. | ①⑤ | C. | ③⑧ | D. | ③⑥⑧ |
9.下列说法不正确的是( )
①有化学键被破坏的变化就是化学变化
②用化学键的强弱可以判断氯化钠与溴化钠,氯化氢与溴化氢的熔沸点高低
③质子数相同的微粒不一定是同种元素
④如果ⅡA族某元素原子序数为x,则同周期ⅢA族的元素的原子序数为x+1
⑤如果三周期某元素原子序数为x,则同主族四周期的元素的原子序数为x+8
⑥ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物酸性越强.
0 163496 163504 163510 163514 163520 163522 163526 163532 163534 163540 163546 163550 163552 163556 163562 163564 163570 163574 163576 163580 163582 163586 163588 163590 163591 163592 163594 163595 163596 163598 163600 163604 163606 163610 163612 163616 163622 163624 163630 163634 163636 163640 163646 163652 163654 163660 163664 163666 163672 163676 163682 163690 203614
①有化学键被破坏的变化就是化学变化
②用化学键的强弱可以判断氯化钠与溴化钠,氯化氢与溴化氢的熔沸点高低
③质子数相同的微粒不一定是同种元素
④如果ⅡA族某元素原子序数为x,则同周期ⅢA族的元素的原子序数为x+1
⑤如果三周期某元素原子序数为x,则同主族四周期的元素的原子序数为x+8
⑥ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物酸性越强.
| A. | ①②④⑤ | B. | ③⑤⑥ | C. | ②④⑥ | D. | ①②④⑤⑥ |



 硫单质及其化合物在工农业生产中有着重要的应用.
硫单质及其化合物在工农业生产中有着重要的应用.