题目内容
9.下列说法不正确的是( )①有化学键被破坏的变化就是化学变化
②用化学键的强弱可以判断氯化钠与溴化钠,氯化氢与溴化氢的熔沸点高低
③质子数相同的微粒不一定是同种元素
④如果ⅡA族某元素原子序数为x,则同周期ⅢA族的元素的原子序数为x+1
⑤如果三周期某元素原子序数为x,则同主族四周期的元素的原子序数为x+8
⑥ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物酸性越强.
| A. | ①②④⑤ | B. | ③⑤⑥ | C. | ②④⑥ | D. | ①②④⑤⑥ |
分析 ①化学键存在化学键的断裂和形成;
②影响分子晶体熔沸点高低的因素是分子间作用力的大小;
③质子数相同的微粒不一定为原子,也可能为离子或原子团;
④元素周期表中,从第四周期开始出现过渡元素,第ⅠA、ⅡA之后是第ⅢB,在第六、七周期中的过渡元素又出现镧系和锕系;
⑤如果三周期某元素原子序数为x,则同主族四周期的元素的原子序数为x+8,也可能相差18;
⑥ⅦA族元素的阴离子还原性越强,对应的元素的非金属性越弱.
解答 解:①仅存在化学键的断裂,则一定不是化学反应,化学键存在化学键的断裂和形成,故错误;
②化学键影响氢化物的稳定性,影响分子晶体熔沸点高低的因素是分子间作用力的大小,故错误;
③质子数相同的微粒不一定为原子,也可能为离子或原子团,如Ne和氨气等,故正确;
④因为是同一周期的IIA族,即同一横行往右一个主族,在第二、三周期原子序数增加1,因而可以x+1;又因为IIA族与IIIA族元素在第四周期起有过渡元素,因而又可以为x+11;在第六、七周期的过渡元素中又出现镧系和锕系,因而又可以为x+25,故错误;
⑤如果三周期某元素原子序数为x,则同主族四周期的元素的原子序数为x+8,也可能相差18,故错误;
⑥ⅦA族元素的阴离子还原性越强,对应的元素的非金属性越弱,其最高价氧化物对应水化物酸性越弱,故错误.
故选D.
点评 本题考查“位构性”、化学键及离子化合物、共价化合物,为高频考点,侧重考查学生的分析能力,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
19.下列图象分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法正确的是( )


| A. | 石墨转变为金刚石是吸热反应 | |
| B. | 白磷比红磷稳定 | |
| C. | S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2,则△H1<△H2 | |
| D. | CO(g)+H2O(g)═CO2(g)+H2(g)△H>0 |
20.下列叙述Ⅰ和Ⅱ均正确并且互为因果关系的是( )
| 选项 | 叙 述Ⅰ | 叙 述Ⅱ |
| A | NH3溶于水显碱性 | 用氨气作“喷泉实验” |
| B | 高锰酸钾具有强氧化性 | 高锰酸钾须与活性金属粉末分开储存 |
| C | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
| D | 碘在酒精中溶解度大于在水中溶解度 | 用酒精萃取碘水中的碘 |
| A. | A | B. | B | C. | C | D. | D |
4.下列说法正确的是( )
| A. | 苯和乙烯均含有碳碳双键,均可使溴的CCl4溶液褪色 | |
| B. | 苯( )的一氯代物有一种,丙烷的一氯代物也有一种 )的一氯代物有一种,丙烷的一氯代物也有一种 | |
| C. | 乙醇和乙烯均可与酸性高锰酸钾发生反应 | |
| D. | 所有的有机物都很容易燃烧 |
14.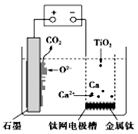 研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金金属钛.下列说法中错误的是
研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金金属钛.下列说法中错误的是
( )
 研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金金属钛.下列说法中错误的是
研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金金属钛.下列说法中错误的是( )
| A. | 阳极的电极反应式为:C+2O2--4e-═CO2↑ | |
| B. | 在制备金属钛前后,整套装置中CaO的总量保持不变 | |
| C. | 若用铅蓄电池作供电电源,“一”接线柱应连接Pb电极 | |
| D. | 由TiO2制得1 mol金属Ti,理论上外电路通过2 mol电子 |
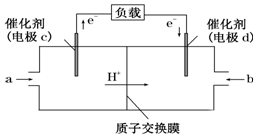
1. 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A. | 该装置将化学能转化为电能 | |
| B. | 电极b附近的pH值增大 | |
| C. | 电子迁移方向:电极a→灯泡→电极b→电解质溶液→电极a | |
| D. | 该电池的总反应:2H2+O2═2H2O |
19.下列说法不正确的是( )
| A. | 硅晶体的导电性介于导体和绝缘体之间,常用作光导纤维 | |
| B. | BaSO4被称为重晶石,可用做“钡餐” | |
| C. | 氧化铁红颜料跟某些油料混合,可以制成防锈油漆 | |
| D. | 钠和钾的合金可用于快中子反应堆作热交换剂 |