13.同主族两种元素原子的核外电子数的差值不可能是( )
| A. | 10 | B. | 18 | C. | 26 | D. | 30 |
12.下列各组气体均可在如图装置中发生喷泉实验的是( )
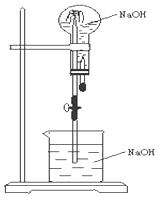

| A. | HCl和CO2 | B. | NH3 和CH4 | C. | SO2 和CO | D. | NO和NO2 |
11.关于化学键的叙述中,下列说法中正确的是( )
| A. | 含有金属元素的化合物一定是离子化合物 | |
| B. | 氢键属于化学键,但比较弱 | |
| C. | 由多种非金属元素组成的化合物一定是共价化合物 | |
| D. | 共价化合物中一定不存在离子键 |
10.X、Y、Z、W是原子序数依次增大的4种短周期元素,X与Z位于同一主族,X原子的最外层电子数是次外层电子数的2倍,Y元素的单质既能与盐酸反应又能与NaOH溶液反应,X、Y、Z、W原子的最外层电子数之和为18.下列说法中不正确的是( )
| A. | X单质在一定条件下能与Z的最高价氧化物发生置换反应 | |
| B. | 原子半径:Y>Z>W | |
| C. | 最高价氧化物对应水化物的酸性由弱到强的顺序:X<Z<W | |
| D. | W的气态氢化物的沸点比氟化氢的沸点低 |
9.下列说法中错误的是( )
| A. | 随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大 | |
| B. | 碱金属元素中,锂原子失去最外层电子的能力最弱 | |
| C. | 钾与水的反应比钠与水的反应更剧烈 | |
| D. | 因为非金属性Cl>S,盐酸的酸性比氢硫酸强 |
8.下列关于元素周期表的说法中正确的是( )
| A. | 过渡元素全部都是副族元素 | |
| B. | 短周期共有20 种元素 | |
| C. | 科学研究时,经常在金属、非金属分界处寻找半导体材料 | |
| D. | 元素周期表共七个横行代表七个周期,18 个纵列代表18 个族 |
7.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).下列可以判断该分解反应已经达到化学平衡状态的是( )
| A. | v(NH3)=2v(CO2) | |
| B. | 密闭容器中混合气体的平均摩尔质量不变 | |
| C. | 密闭容器中混合气体密度不变 | |
| D. | 密闭容器中氨气的体积分数不变 |
5.S(单斜)和S(正交)是硫的两种同素异形体.已知:
①S(s,单斜)+O2(g)═SO2(g)△H1=-297.16kJ•mol-1
②S(s,正交)+O2(g)═SO2(g)△H2=-296.83kJ•mol-1
③S(s,单斜)═S(s,正交)△H3.
下列说法正确的是( )
①S(s,单斜)+O2(g)═SO2(g)△H1=-297.16kJ•mol-1
②S(s,正交)+O2(g)═SO2(g)△H2=-296.83kJ•mol-1
③S(s,单斜)═S(s,正交)△H3.
下列说法正确的是( )
| A. | S(s,单斜)═S(s,正交)△H3<0,正交硫比单斜硫稳定 | |
| B. | 单斜硫转化为正交硫的反应是吸热反应 | |
| C. | △H3=+0.33 kJ•mol-1 | |
| D. | S(s,单斜)═S(s,正交)△H3>0,单斜硫比正交硫稳定 |
4.关于化学键的下列叙述中,正确的是( )
0 163433 163441 163447 163451 163457 163459 163463 163469 163471 163477 163483 163487 163489 163493 163499 163501 163507 163511 163513 163517 163519 163523 163525 163527 163528 163529 163531 163532 163533 163535 163537 163541 163543 163547 163549 163553 163559 163561 163567 163571 163573 163577 163583 163589 163591 163597 163601 163603 163609 163613 163619 163627 203614
| A. | 离子化合物可能含共价健 | |
| B. | 离子化合物中一定不含共价键,阳离子只能是金属离子 | |
| C. | 共价化合物可能含离子键 | |
| D. | 有化学键断裂就一定有化学键形成 |

 →
→ .
.