题目内容
7.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).下列可以判断该分解反应已经达到化学平衡状态的是( )| A. | v(NH3)=2v(CO2) | |
| B. | 密闭容器中混合气体的平均摩尔质量不变 | |
| C. | 密闭容器中混合气体密度不变 | |
| D. | 密闭容器中氨气的体积分数不变 |
分析 化学平衡状态的特征是:当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A.反应则速率之比等于化学方程式计量数之比为正反应速率之比,v(NH3)=2v(CO2)不能说明正逆反应速率相同,故A错误;
B.反应物为固体生成物为气体,气体平均摩尔质量始终不变,不能说明反应达到平衡状态,故B错误;
C.反应前后气体质量不变,体积不变,则密闭容器中混合气体密度不变,能说明正逆反应速率相同反应达到平衡状态,故C正确;
D.反应物为固体,生成的氨气在混合气体中体积分数始终不变,不能说明反应达到平衡状态,故D错误;
故选C.
点评 本题考查了化学平衡状态的判断,题目难度不大,注意当反应达到平衡状态时,正逆反应速率相等是判断的实质.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | 所有共价键都有方向性 | |
| B. | s轨道和p轨道重叠可以形成π键 | |
| C. | 若把H2S分子写成H3S分子,违背了共价键的饱和性 | |
| D. | 两个原子之间形成共价键时,可形成多个σ键 |
15.下列反应中,既属于氧化还原反应且为放热反应的是( )
| A. | 氢氧化钾与硫酸的反应 | |
| B. | 金属镁与盐酸的反应 | |
| C. | 高温条件下碳粉与二氧化碳的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl固体的反应 |
2.下列表达方式错误的是( )
| A. | 氟化钠的电子式为  | B. | 氯原子的结构示意图: | ||
| C. | CO2分子的结构式:O=C=O | D. | 甲烷的电子式  |
12.下列各组气体均可在如图装置中发生喷泉实验的是( )
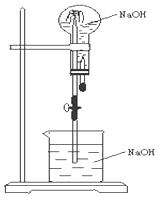

| A. | HCl和CO2 | B. | NH3 和CH4 | C. | SO2 和CO | D. | NO和NO2 |
16.分别取等质量的两种烃完全燃烧,生成CO2及消耗O2的量均相同,这两种烃之间的关系正确的是( )
| A. | 只能是同种物质 | B. | 一定是同系物,有相同的通式 | ||
| C. | 实验式一定相同 | D. | 一定互为同分异构体 |
17.下列变化中,属于物理变化的是( )
| A. | 从石油中分馏出汽油 | B. | 煤的气化制水煤气 | ||
| C. | 煤的干馏制焦炭 | D. | 油脂的水解制肥皂 |
 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验
