题目内容
11.关于化学键的叙述中,下列说法中正确的是( )| A. | 含有金属元素的化合物一定是离子化合物 | |
| B. | 氢键属于化学键,但比较弱 | |
| C. | 由多种非金属元素组成的化合物一定是共价化合物 | |
| D. | 共价化合物中一定不存在离子键 |
分析 离子化合物中一般为活泼金属与非金属形成的化合物,包括强碱、大多数盐,一定含有离子键,可能含有共价键,共价化合物中只含共价键,一定不含离子键,以此解答该题.
解答 解:A.氯化铝为共价化合物,故A错误;
B.氢键属于分子间作用力,故B错误;
C.铵盐由非金属元素组成,但为离子化合物,故C错误;
D.离子键只存在于离子化合物中,故D正确.
故选D.
点评 本题考查化合物和化学键的关系,为高频考点,侧重概念理解的考查,明确共价化合物和离子化合物的概念是解本题关键,注意二者的区别,难度不大.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案
相关题目
2.为了更简便地制取干燥的NH3,下列方法中合适的是( )
| A. | N2+3H2$?_{催化剂}^{高温、高压}$2NH3,用烧碱进行干燥 | |
| B. | 加热NH4HCO3,气体用五氧化二磷干燥 | |
| C. | 加热浓氨水,气体用碱石灰干燥 | |
| D. | 2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O,气体用无水氯化钙干燥 |
2. 金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的 电源.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能.下列说法不正确的是( )
金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的 电源.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能.下列说法不正确的是( )
 金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的 电源.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能.下列说法不正确的是( )
金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的 电源.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能.下列说法不正确的是( )| A. | 采用多孔电极的目的是提高电极与电解质溶液 的接触面积,并有利于氧气扩散至电极表面 | |
| B. | M-空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne-═4M(OH)n | |
| C. | 比较 Mg、Al、Zn 三种金属-空气电池,Al-空气电池的理论比能量最高 | |
| D. | 在 Mg-空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 |
19.下列物质在空气中不易变质的是( )
| A. | FeSO4 | B. | NaClO | C. | Na2SiO3 | D. | NaHSO4 |
16.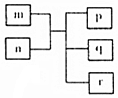 短周期主族元素X、Y、Z、W原子序数依次递增,Y原子最外层电子数为次外层电子数的二倍.m为元素Y的单质,n为元素Z的最高价氧化物的水化物,p、q、r分别为上述四种元素组成的二元化合物.下列说法正确的是( )
短周期主族元素X、Y、Z、W原子序数依次递增,Y原子最外层电子数为次外层电子数的二倍.m为元素Y的单质,n为元素Z的最高价氧化物的水化物,p、q、r分别为上述四种元素组成的二元化合物.下列说法正确的是( )
 短周期主族元素X、Y、Z、W原子序数依次递增,Y原子最外层电子数为次外层电子数的二倍.m为元素Y的单质,n为元素Z的最高价氧化物的水化物,p、q、r分别为上述四种元素组成的二元化合物.下列说法正确的是( )
短周期主族元素X、Y、Z、W原子序数依次递增,Y原子最外层电子数为次外层电子数的二倍.m为元素Y的单质,n为元素Z的最高价氧化物的水化物,p、q、r分别为上述四种元素组成的二元化合物.下列说法正确的是( )| A. | 原子半径Y<Z<W | |
| B. | 简单气态氢化物的稳定性Y>Z>W | |
| C. | X与Z形成的化合物的水溶液一定为酸性溶液 | |
| D. | X、Z、W三种元素可以形成离子化合物 |
3.具有下列原子序数的各组元素,能组成化学式AB2型化合物,并且该化合物在固态时为原子晶体的是( )
| A. | 6和8 | B. | 20和17 | C. | 14和8 | D. | 6和16 |
20.大海是一个资源宝库,从海水中提取镁和溴的实验如下:
Ⅰ.(1)海水提镁的步骤如下,请在横线上将实验步骤、目的补充完整.
(2)结合以上实验步骤,列举一个能与海水提镁相联合的工业生产实例制备盐酸.
Ⅱ.已知海水中溴元素主要以Br-形式存在,工业上从海水中提取溴的流程如下:

(1)吸收塔1中发生反应的离子方程式为Cl2+2Br-=Br2+2Cl-.
(2)吸收塔2中发生反应:3Br2+3Na2CO3=NaBrO3+3CO2+5NaBr.当3mol Br2完全反应时转移电子5mol.
(3)吸收塔3中反应的离子方程式为5Br-+BrO3-+6H+=Br2+3H2O.
(4)吹出塔、吸收塔2的作用分别是用热空气把生成的溴单质吹出,富集溴.
Ⅰ.(1)海水提镁的步骤如下,请在横线上将实验步骤、目的补充完整.
| 实验步骤 | 实验目的 |
| ①将贝壳煅烧后制成石灰乳. | |
| ②将海水进行浓缩. | |
| ③加入石灰乳沉淀过滤. | 沉淀镁离子生成氢氧化镁沉淀 |
| ④向步骤③所得物质中加入稀盐酸,将溶液进行蒸发浓缩、结晶、过滤. | |
| ⑤将得到的产物干燥除水后,MgCl2 $\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑(填化学方程式)得到金属镁. |
Ⅱ.已知海水中溴元素主要以Br-形式存在,工业上从海水中提取溴的流程如下:

(1)吸收塔1中发生反应的离子方程式为Cl2+2Br-=Br2+2Cl-.
(2)吸收塔2中发生反应:3Br2+3Na2CO3=NaBrO3+3CO2+5NaBr.当3mol Br2完全反应时转移电子5mol.
(3)吸收塔3中反应的离子方程式为5Br-+BrO3-+6H+=Br2+3H2O.
(4)吹出塔、吸收塔2的作用分别是用热空气把生成的溴单质吹出,富集溴.
1.某化学反应的反应物浓度在20s内由3.0mol/L变为1.0mol/L,则以该反应物浓度的变化表示20s内的平均反应速率为( )
| A. | 0.05 mol/(L•s) | B. | 0.10 mol/(L•s) | C. | 0.15 mol/(L•s) | D. | 2.0 mol/(L•s) |

 →
→ .
.