7. 过氧化氢(H2O2)俗称双氧水.是一种重要的化工产品,具有漂白、氧化、消毒、杀菌等多种功效,广泛应用于纺织、造纸、化工、电子、轻工、污水处理等工业.回答下列问题:
过氧化氢(H2O2)俗称双氧水.是一种重要的化工产品,具有漂白、氧化、消毒、杀菌等多种功效,广泛应用于纺织、造纸、化工、电子、轻工、污水处理等工业.回答下列问题:
(1)H2O2的电子式为 .
.
(2)用H2O2与稀硫酸的混合溶液可溶出印刷电路板金属粉末中的铜.
已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64kJ/mol
2H2O2(1)═2H2O(l)+O2(g)△H=-196kJmol
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-286kJ/mol
则在稀硫酸溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-320kJ/mol.
(3)工业上常用电解硫酸氢铵水溶液的方法制备过氧化氢,其原理为:首先2NH4HSO4$\frac{\underline{\;通电\;}}{\;}$(NH4)2S2O8+H2↑,然后由(NH4)2S2O8水解得到H2O2和另一产物.则:
①电解时阳极的电极反应式为2SO42--2e-=S2O82-;
②(NH4)2S2O8水解时发生反应的化学方程式为(NH4)2S2O8+2H2O=2NH4HSO4+H2O2.
(4)现甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素(仅一个条件改变).甲小组有如下实验设计方案.
甲、乙两小组得出如图数据.
①甲小组实验得出的结论是H2O2分解时,MnO2比Fe2O3催化效率更高.
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析,相同条件下H2O2在碱(填“酸”或“碱”)性环境下放出气体速率较快;由此,乙组提出可以用BaO2固体与硫酸溶液反应制H2O2,其反应的离子方程式为BaO2+2H++SO42-═BaSO4↓+H2O2;支持这一方案的理由是(BaSO4的生成有利于平衡右移即有利于H2O2的生成)酸性环境有利于H2O2的存在(等其他合理原因).
③已知过氧化氢还是一种极弱的二元酸:H2O2?H++HO2-(K${\;}_{{a}_{1}}$=2.4×10-12).当稀H2O2溶液在碱性环境下分解时会发生反应H2O2+OH-?HO2-+H2O,该反应中,正反应速率为V正=k正•c(H2O2)•c(OH-),逆反应速率为v逆=k逆•c(H2O)•c(HO2-),其中k正、k逆为速率常数,则k正与k逆的比值为1.33×104(保留3位有效数字).
 过氧化氢(H2O2)俗称双氧水.是一种重要的化工产品,具有漂白、氧化、消毒、杀菌等多种功效,广泛应用于纺织、造纸、化工、电子、轻工、污水处理等工业.回答下列问题:
过氧化氢(H2O2)俗称双氧水.是一种重要的化工产品,具有漂白、氧化、消毒、杀菌等多种功效,广泛应用于纺织、造纸、化工、电子、轻工、污水处理等工业.回答下列问题:(1)H2O2的电子式为
 .
.(2)用H2O2与稀硫酸的混合溶液可溶出印刷电路板金属粉末中的铜.
已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64kJ/mol
2H2O2(1)═2H2O(l)+O2(g)△H=-196kJmol
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-286kJ/mol
则在稀硫酸溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-320kJ/mol.
(3)工业上常用电解硫酸氢铵水溶液的方法制备过氧化氢,其原理为:首先2NH4HSO4$\frac{\underline{\;通电\;}}{\;}$(NH4)2S2O8+H2↑,然后由(NH4)2S2O8水解得到H2O2和另一产物.则:
①电解时阳极的电极反应式为2SO42--2e-=S2O82-;
②(NH4)2S2O8水解时发生反应的化学方程式为(NH4)2S2O8+2H2O=2NH4HSO4+H2O2.
(4)现甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素(仅一个条件改变).甲小组有如下实验设计方案.
| 实验编号 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 25℃ | 三氧化二铁 | 10mL5%H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
①甲小组实验得出的结论是H2O2分解时,MnO2比Fe2O3催化效率更高.
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析,相同条件下H2O2在碱(填“酸”或“碱”)性环境下放出气体速率较快;由此,乙组提出可以用BaO2固体与硫酸溶液反应制H2O2,其反应的离子方程式为BaO2+2H++SO42-═BaSO4↓+H2O2;支持这一方案的理由是(BaSO4的生成有利于平衡右移即有利于H2O2的生成)酸性环境有利于H2O2的存在(等其他合理原因).
③已知过氧化氢还是一种极弱的二元酸:H2O2?H++HO2-(K${\;}_{{a}_{1}}$=2.4×10-12).当稀H2O2溶液在碱性环境下分解时会发生反应H2O2+OH-?HO2-+H2O,该反应中,正反应速率为V正=k正•c(H2O2)•c(OH-),逆反应速率为v逆=k逆•c(H2O)•c(HO2-),其中k正、k逆为速率常数,则k正与k逆的比值为1.33×104(保留3位有效数字).
6.纵观古今,化学与生活皆有着密切联系.下列有关说法错误的是( )
| A. | 陶瓷是中华民族祖先的一项伟大发明,烧结黏土制陶瓷的过程不涉及化学反应 | |
| B. | 制作烟花的过程中常加入金属发光剂和发色剂使烟花放出五彩缤纷的颜色 | |
| C. | “水滴石穿”主要是溶解了的雨水对石灰石的溶解作用 | |
| D. | 严格地讲通风橱”是一种不负责任的防污染手段,因为实验产生的有害气体没有得到转化或吸收 |
5.下列有关“化学与生活”的叙述正确的是( )
| A. | Fe(OH)3胶体无色、透明,能产生丁达尔现象 | |
| B. | 六水氯化钙可用作食品干燥剂 | |
| C. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| D. | 用含硅胶、铁粉的透气小袋与食品一起密封包装,该过程没有发生化学反应 |
3.下列关于第一电离能大小的比较正确的是( )
| A. | K>Ca>Ga | B. | Li>Na>K | C. | S>P>Al | D. | H>N>Ne |
1.下列烃充分燃烧后,生成二氧化碳和水的物质的量之比等于1:2的是( )
| A. | 甲烷 | B. | 乙烯 | C. | 丙烷 | D. | 丙烯 |
20.为了检验某氯化烃中的氯元素,现进行如下操作.其中合理的是( )
| A. | 取氯代烃少许,加入AgNO3溶液 | |
| B. | 取氯代烃少许与NaOH水溶液共热,然后加入AgNO3溶液 | |
| C. | 取氯代烃少许与NaOH水溶液共热后,加入稀硝酸酸化,再加入AgNO3 | |
| D. | 取氯代烃少许与NaOH乙醇溶液共热后,加入稀硝酸酸化,再加入AgNO3溶液 |
19.若某ⅡB族元素原子序数为x,那么原子序数为x+1的元素位于周期表中的( )
| A. | ⅢB族 | B. | ⅢA族 | C. | ⅤⅢ族 | D. | 0族 |
18.若把元素周期表原来的主副族及族号取消,从左到右共有18列,则下列说法中错误的是( )
0 163019 163027 163033 163037 163043 163045 163049 163055 163057 163063 163069 163073 163075 163079 163085 163087 163093 163097 163099 163103 163105 163109 163111 163113 163114 163115 163117 163118 163119 163121 163123 163127 163129 163133 163135 163139 163145 163147 163153 163157 163159 163163 163169 163175 163177 163183 163187 163189 163195 163199 163205 163213 203614
| A. | 第17列为卤族元素 | |
| B. | 第9列元素中没有非金属元素 | |
| C. | 只有第2列元素原子的最外层有2个电子 | |
| D. | 在整个18列元素中,第3列元素种类最多 |
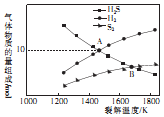 硫化氢是天然气及石油中的含硫杂质,近年来发现H2S可用于高效制取氢气.
硫化氢是天然气及石油中的含硫杂质,近年来发现H2S可用于高效制取氢气.