题目内容
18.若把元素周期表原来的主副族及族号取消,从左到右共有18列,则下列说法中错误的是( )| A. | 第17列为卤族元素 | |
| B. | 第9列元素中没有非金属元素 | |
| C. | 只有第2列元素原子的最外层有2个电子 | |
| D. | 在整个18列元素中,第3列元素种类最多 |
分析 在长式周期表中各族元素的排列顺序为:ⅠA、ⅡA、ⅢB-→ⅦB、Ⅷ、ⅠB、ⅡB、ⅢA-→ⅦA、0族,18列元素应分别与以上各族对应.
A.第17列为卤素;
B.第9列元素为第Ⅷ族元素;
C.He以及ⅡB族元素最外层都为2电子;
D.第3列含有锕系、镧系元素.
解答 解:在长式周期表中各族元素的排列顺序为:ⅠA、ⅡA、ⅢB-→ⅦB、Ⅷ、ⅠB、ⅡB、ⅢA-→ⅦA、0族,18列元素应分别与以上各族对应.
A.第17列为卤素,故A正确;
B.第9列元素为第Ⅷ族元素,属于过度金属元素,故B正确;
C.第2列为碱土金属族,其最外层有2个电子,但元素He及多数过渡元素的最外层也是2个电子,故C错误;
D.第3列含有锕系、镧系元素,元素种类最多,故D正确.
故选C.
点评 本题考查了长式周期表中各族元素的排列顺序,明确列与族序数的排列顺序即可解答,题目难度不大,注意选项C中的特例分析.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
15.关于下列图象的描述不正确的是( )

| A. | 图①可以表示在绝热容器中放入N2和H2,在催化合成氮的过程中,N2的转化率随时间的变化曲线 | |
| B. | 图②可以表示在T℃的密闭容器中,反应2AgBr(s)?2Ag(s)+Br2(g)达到平衡,此时再开始增大容器的体积,最终容器中仍有AgBr(s)剩余时容器内压强的变化曲线 | |
| C. | 图③可以表示等体积等pH的碳酸钠溶液和醋酸钠溶液加水稀释过程中pH的变化趋势 | |
| D. | 图④可以表示氯化银和溴化银饱和溶液等体积混合后,再向该混合溶液中加入浓AgNO3溶液时,生成沉淀的物质的量随加入AgNO3溶液体积的变化曲线 |
16.设NA是阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 4.6g NO2(g)和N2O4(g)的混合物中含有0.3NA个原子 | |
| B. | 0.1mol乙酸与足量乙醇发生酯化反应,生成0.1NA个乙酸乙酯分子 | |
| C. | 常温下将5.6gFe投入足量浓硫酸,电子转移数为0.3NA | |
| D. | Na2O2与足量H2O发生反应,每生成2.24L气体(标准状况),电子转移数0.4NA |
6.25℃时,有amLpH=9的氨水(A)和bmLpH=10的氨水(B),cmLpH=10的NaOH溶液(C),它们能中和同量的盐酸.以下叙述正确的是( )
| A. | 与等量盐酸恰好中和时放出的热量:A=B | |
| B. | 与等量盐酸恰好中和时所得溶液的pH:A=B=C | |
| C. | a>10b | |
| D. | A和B相比,氨水A中$\frac{c(N{H}_{3}•{H}_{2}O)c({H}^{+})}{c(N{{H}_{4}}^{+})}$较小 |
13.下列原子的价电子排布正确的是( )
| A. | N: | B. | O: | ||
| C. | C: | D. | F: |
3.下列关于第一电离能大小的比较正确的是( )
| A. | K>Ca>Ga | B. | Li>Na>K | C. | S>P>Al | D. | H>N>Ne |
7.化学与生活密切相关,下列叙述中不正确的是( )
| A. | 复方氢氧化铝有中和胃酸、解痉止痛的作用,胃痛、胃酸过多的患者可大量服用 | |
| B. | 食盐可作调味剂,也可作食品防腐剂 | |
| C. | 天然存在的动植物油脂几乎都是混合物,没有固定的熔沸点 | |
| D. | 硫化氢是空气污染物,有臭鸡蛋气味,有剧毒 |
8.有机物M、N、Q的转化关系为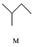 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$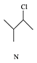 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$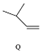 ,下列说法正确的是( )
,下列说法正确的是( )
 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ ,下列说法正确的是( )
,下列说法正确的是( )| A. | M的名称为异丁烷 | |
| B. | N的同分异构体有7种(不考虑立体异构,不包括本身) | |
| C. | Q可与溴水反应生成N | |
| D. | M、N、Q均能使酸性KMnO4溶液褪色 |