4.T1℃时.在2L的密闭容器中,反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0达到平衡,反应过程中部分数据见下表.下列说法正确的是( )
| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应I 恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ 绝热恒容 | 0min | 0 | 0 | 2 | 2 |
| A. | 达到平衡时,反应Ⅰ、Ⅱ对比,平衡常数:K(Ⅰ)>K(Ⅱ) | |
| B. | 对于反应Ⅰ,前10min内的平均反应速率v(CH3OH)=0.025mol•L-1•min-1 | |
| C. | 对于反应Ⅰ,若30min时只改变温度为T2℃,再次达到平衡时H2的物质的量为3.2mol,则T1>T2 | |
| D. | 对于反应Ⅰ,若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡正向移动 |
3.联苯(结构如图所示 ),碳碳单键可以旋转)的二氯代物有( )
),碳碳单键可以旋转)的二氯代物有( )
 ),碳碳单键可以旋转)的二氯代物有( )
),碳碳单键可以旋转)的二氯代物有( )| A. | 9种 | B. | 12种 | C. | 20种 | D. | 24种 |
2.在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入1L的密闭容器中发生反应:
CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=akJ/mol.测得有关数据如表:
下列说法正确的是( )
CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=akJ/mol.测得有关数据如表:
| 温度 | 时间/min 物质的量 | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
| A. | T1>T2,且a>0 | |
| B. | 当温度为T2、反应进行到40 min时,x>0.15 | |
| C. | 温度为T2时,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,重新达到平衡时,n(N2)=0.70mol | |
| D. | 温度为T1时,达平衡时CH4 的转化率大于NO2的转化率 |
12.下列叙述正确的是( )
| A. | NO是具有刺激性的红棕色气体 | |
| B. | SO3溶于水生成亚硫酸 | |
| C. | 向品红溶液中通入二氧化硫气体,溶液褪色,加热后溶液又会出现红色 | |
| D. | 氨水中滴入酚酞溶液,颜色变蓝 |
11.一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示,下列说法正确的是( )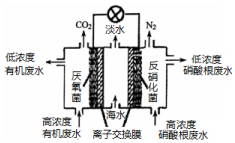

| A. | 该电池能在高温下工作 | |
| B. | 该电池工作时,中间室中的Cl-移向右室 | |
| C. | 正极上发生的电极反应:2NO3-+6H2O+10e-═N2↑+12OH- | |
| D. | 若有机废水中有机物用C6H12O6表示,每消耗1 mol C6H12O6转移4 mol电子 |
10.在给定的条件下,下列选项所示的物质间转化均能实现的是( )
| A. | FeS2$\stackrel{O_{2}/高温}{→}$SO2$\stackrel{H_{2}O_{2}(aq)}{→}$H2SO4 | |
| B. | Cu2(OH)2CO3$\stackrel{H_{2}SO_{4}}{→}$CuSO4(aq)$\stackrel{Na}{→}$Cu | |
| C. | MgCl2(aq)$\stackrel{△}{→}$MgCl2(s)$\stackrel{电解}{→}$Mg | |
| D. | 1mol•L-1HCl(aq)$\stackrel{MnO_{2}/△}{→}$Cl2$\stackrel{石灰乳}{→}$Ca(ClO)2 |
9.利用合成气(主要成分为CO、CO2和H2)通过下列反应合成甲醇.下列说法正确的是( )
反应①:CO2(g)+H2(g)?CO(g)+H2O(g)△H1=41kJ•mol-1
反应②:CO(g)+2H2(g)?CH3OH(g)△H2=-99kJ•mol-1
反应③:CO2(g)+3H2(g)?CH3OH(g)+H2O(l)△H3.
反应①:CO2(g)+H2(g)?CO(g)+H2O(g)△H1=41kJ•mol-1
反应②:CO(g)+2H2(g)?CH3OH(g)△H2=-99kJ•mol-1
反应③:CO2(g)+3H2(g)?CH3OH(g)+H2O(l)△H3.
| A. | 反应①为放热反应 | B. | 增大反应①的压强,H2转化率提高 | ||
| C. | 反应②使用催化剂,△H2不变 | D. | △H3=-58 KJ•mol-1 |
8.短周期主族元素X、Y、Z、W的原子序数依次增大,X元素原子最外层电子数是内层的2倍,Y是地壳中含量最高的元素,W的原子序数是Y的2倍,X、Y、Z、W最外层电子数之和为19.下列说法正确的是( )
| A. | X和Y只能形成一种化合物 | |
| B. | 原子半径:r(Z)>r(W)>r(Y) | |
| C. | W的简单气态氢化物的热稳定性比Y强 | |
| D. | 元素Z、W的简单离子具有相同的电子层结构 |
7.原子序数依次增大的四种短周期元素X、Y、Z、W,X的最高正化合价与Z的相同,Z原子的最外层电子数是内层电子数的0.4倍,Y元素的周期序数等于族序数,W的最高价氧化物对应的水化物的浓溶液Q是实验室常用的气体干燥剂.下列说法错误的是( )
0 163006 163014 163020 163024 163030 163032 163036 163042 163044 163050 163056 163060 163062 163066 163072 163074 163080 163084 163086 163090 163092 163096 163098 163100 163101 163102 163104 163105 163106 163108 163110 163114 163116 163120 163122 163126 163132 163134 163140 163144 163146 163150 163156 163162 163164 163170 163174 163176 163182 163186 163192 163200 203614
| A. | 原子半径:Y>Z>W>X | B. | 简单气态氢化物的热稳定性:X>Z | ||
| C. | 野外钢轨焊接中常用到Y的单质 | D. | 加热条件下Q可氧化X、Y、Z的单质 |
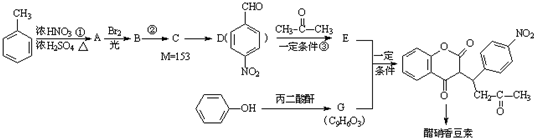

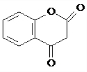 .
.