题目内容
9.利用合成气(主要成分为CO、CO2和H2)通过下列反应合成甲醇.下列说法正确的是( )反应①:CO2(g)+H2(g)?CO(g)+H2O(g)△H1=41kJ•mol-1
反应②:CO(g)+2H2(g)?CH3OH(g)△H2=-99kJ•mol-1
反应③:CO2(g)+3H2(g)?CH3OH(g)+H2O(l)△H3.
| A. | 反应①为放热反应 | B. | 增大反应①的压强,H2转化率提高 | ||
| C. | 反应②使用催化剂,△H2不变 | D. | △H3=-58 KJ•mol-1 |
分析 A.△H>0的反应为吸热反应;
B.反应①中,反应前后气体的体积不变;
C.加入催化剂,不改变反应热;
D.由盖斯定律将①+②可得CO2(g)+3H2(g)?CH3OH(g)+H2O(g),气体变为液体放出热量.
解答 解:A.反应①的△H>0,为吸热反应,故A错误;
B.反应①中,反应前后气体的体积不变,则增大压强,平衡不移动,氢气的转化率不变,故B错误;
C.加入催化剂,可降低反应的活化能,但不改变反应热,故C正确;
D.由盖斯定律将①+②可得CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H=-58 KJ•mol-1,气体变为液体放出热量,则CO2(g)+3H2(g)?CH3OH(g)+H2O(l)△H3<-58 KJ•mol-1,故D错误.
故选C.
点评 本题考查化学反应与能量变化,为高频考点,侧重考查学生的分析能力,主要把握盖斯定律的运用,理解外界条件对平衡移动的影响,难度不大.

练习册系列答案
相关题目
20.X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g•L-1,W在短周期主族元素中原子半径最大.下列说法不正确的是( )
| A. | 原子半径:W>Y>M | |
| B. | 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 | |
| C. | W和Z形成的化合物中阴、阳离子物质的量之比均为1:2 | |
| D. | X的单质可由金属单质置换得到 |
17.室温下,将0.05molCH3COONa固体溶于水配成100mL溶液,向溶液中加入下列物质充分混合后,有关结论不正确的是( )
| 加入的物质 | 结论 | |
| A | 0.05molCH3COONa固体 | $\frac{c(C{H}_{3}CO{O}^{-})}{c(N{a}^{+})}$减小 |
| B | 0.05molNaHSO4固体 | C(CH3COO-)+c(CH3COOH)=c(Na+)-c(SO42-) |
| C | 0.05molNH4Cl固体 | 水电离程度增大 |
| D | 50mLH2O | 由水电离出的c(H+)c(OH-)减小 |
| A. | A | B. | B | C. | C | D. | D |
4.短周期主族元素X、Y、Z、W的原子序数依次增大,X、W同主族;Y、Z同周期;X、Y、Z三种元素形成一种化合物M,25℃时,0.1mol•L-1的M溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1.0×10-12.下列说法正确的是( )
| A. | 简单离子半径:Y<Z<W | |
| B. | X分別与Z、W形成的化合物中,所含化学键类型相同 | |
| C. | X、Y形成的最简单化合物的电子式为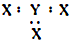 | |
| D. | Z分別与X、W均可形成具有漂白性的化合物 |
2.在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入1L的密闭容器中发生反应:
CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=akJ/mol.测得有关数据如表:
下列说法正确的是( )
CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=akJ/mol.测得有关数据如表:
| 温度 | 时间/min 物质的量 | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
| A. | T1>T2,且a>0 | |
| B. | 当温度为T2、反应进行到40 min时,x>0.15 | |
| C. | 温度为T2时,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,重新达到平衡时,n(N2)=0.70mol | |
| D. | 温度为T1时,达平衡时CH4 的转化率大于NO2的转化率 |
9.下列反应中属于放热反应而且是氧化还原反应的是( )
| A. | 铝粉与氧化铁粉末反应 | B. | 强酸与强碱的中和反应 | ||
| C. | 碳酸钙受热分解 | D. | 氧化钙溶于水 |
6.对于放热反应A2+B2═C2,下列说法正确的是( )
| A. | 产物C2所具有的总能量高于反应物A2和B2所具有的总能量 | |
| B. | 反应物A2和B2所具有的总能量高于产物C2所具有的总能量 | |
| C. | 破坏A2和B2分子内的化学键所吸收的总能量高于形成C2分子内的化学键所放出的总能量 | |
| D. | 破坏A2和B2分子内的化学键所放出的总能量高于形成C2分子内的化学键所吸收的总能量 |
7.实验室以蛇纹石酸浸出液(主要含Fe3+,还有一定量的Al3+、Mn2+、Ca2+、Mg2+等)为原料制备高纯氧化铁,流程如图1:
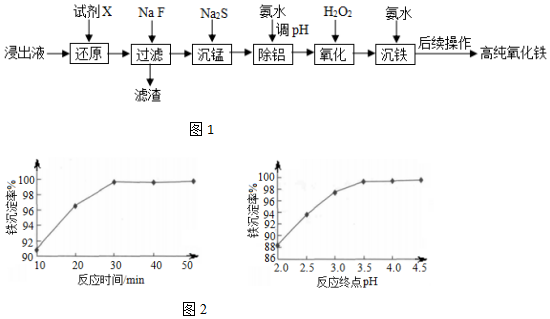
已知流程中相关金属离子生成氢氧化物沉淀的pH如表:
(1)“还原”时,应选择C(填字母).
A.Zn粉 B.NaClO溶液 C.Fe粉
(2)“滤渣”的主要成分除含有少量MnF2外,还含有CaF2、MgF2(填化学式).
(3)“沉锰”时,已知:Ksp(MnS)=4.65×10-14.为确保沉锰完全[即溶液中c(Mn2+)<1.0×10-6 mol•L-1],应保持溶液中c(S2-)>4.65×10-8mol•L-1mol•L-1.
(4)“除铝”时,控制溶液pH的范围为5.0~5.8.
(5)“氧化”时,常用酸性K2Cr2O7溶液检测是否残留未被氧化的金属离子,该反应的离子方程式为Cr2O72-+14H++6Fe2+═2Cr3++6Fe3++7H2O.
(6)“沉铁”时,反应温度为85℃条件下,反应时间和反应终点pH对铁的沉淀率的影响分别如图2所示,则最佳的工艺条件是反应时间30min、终点pH=3.5.

已知流程中相关金属离子生成氢氧化物沉淀的pH如表:
| 氢氧化物 | Fe3+ | Fe2+ | Al3+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 |
| 沉淀完全的pH | 3.2 | 8.8 | 5.0 |
A.Zn粉 B.NaClO溶液 C.Fe粉
(2)“滤渣”的主要成分除含有少量MnF2外,还含有CaF2、MgF2(填化学式).
(3)“沉锰”时,已知:Ksp(MnS)=4.65×10-14.为确保沉锰完全[即溶液中c(Mn2+)<1.0×10-6 mol•L-1],应保持溶液中c(S2-)>4.65×10-8mol•L-1mol•L-1.
(4)“除铝”时,控制溶液pH的范围为5.0~5.8.
(5)“氧化”时,常用酸性K2Cr2O7溶液检测是否残留未被氧化的金属离子,该反应的离子方程式为Cr2O72-+14H++6Fe2+═2Cr3++6Fe3++7H2O.
(6)“沉铁”时,反应温度为85℃条件下,反应时间和反应终点pH对铁的沉淀率的影响分别如图2所示,则最佳的工艺条件是反应时间30min、终点pH=3.5.
 )分子中碳原子轨道的杂化类型是sp2和sp3,1mol 丙酮分子中含有σ键的数目为9NA.
)分子中碳原子轨道的杂化类型是sp2和sp3,1mol 丙酮分子中含有σ键的数目为9NA.