14. H2S是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为质子膜H2S燃料电池的示意图.下列说法错误的是( )
H2S是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为质子膜H2S燃料电池的示意图.下列说法错误的是( )
 H2S是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为质子膜H2S燃料电池的示意图.下列说法错误的是( )
H2S是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为质子膜H2S燃料电池的示意图.下列说法错误的是( )| A. | 电池工作时,电子从电极a经负载流向电极b | |
| B. | 实际工作中当反应生成64gS2时,电池内部释放632kJ电能 | |
| C. | 电极a上发生的电极反应为:2H2S-4e-=S2+4H+ | |
| D. | 当电路中通过4mol电子时,有4mol H+经质子膜进入正极区 |
12.下列关于能源的叙述错误的是( )
| A. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| B. | 氢氧燃料电池工作过程中,热能转变为电能 | |
| C. | 电解水制取H2过程中,电能转变为化学能 | |
| D. | 生物质能源是可再生能源 |
11.根据热化学方程式(在101kPa时):S(s)+O2(g)=SO2(g)△H=-297.23kJ/mol,分析下列说法中错误的是( )
| A. | S的燃烧热为297.23 kJ/mol | |
| B. | 形成1 mol SO2的化学键所释放的总能量大于断裂1mol S(s)和1mol O2(g)的化学键所吸收的总能量 | |
| C. | S(g)+O2(g)=SO2(g)放出的热量小于297.23 kJ | |
| D. | 1mol SO2的总能量小于 1mol S(s)和1mol O2(g)的总能量 |
10.下列说法错误的是( )
| A. | 化学变化过程中一定伴随着能量变化 | |
| B. | 放热反应可能需要加热才能进行 | |
| C. | 吸热反应只能在加热条件下才能进行 | |
| D. | 天然气在空气中燃烧时,能量转化形式不止一种 |
9.下列叙述与结论均正确的是( )
| A. | 由于硅处于金属与非金属的过渡位置,故硅可用作半导体材枓 | |
| B. | 由于F元素的最低化合价为-1价,故F元素的最高化合价为+7价 | |
| C. | 由于分子中氢原子数:H2SO4>HClO4,故酸性:H2SO4>HClO4 | |
| D. | 由于H2S的相对分子质量大于H2O的相对分子质量,所以沸点前者大于后者 |
8.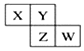 如图所示X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示.若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是( )
如图所示X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示.若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是( )
 如图所示X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示.若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是( )
如图所示X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示.若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是( )| A. | X、Y对应的氧化物都是酸性氧化物 | |
| B. | X的氧化物不能与Mg发生化学反应 | |
| C. | Z比Y更容易与氢气化合 | |
| D. | W与X形成的化合物中化学键类型为共价键 |
7.下列有关原子结构和元素周期律的叙述正确的是( )
0 162934 162942 162948 162952 162958 162960 162964 162970 162972 162978 162984 162988 162990 162994 163000 163002 163008 163012 163014 163018 163020 163024 163026 163028 163029 163030 163032 163033 163034 163036 163038 163042 163044 163048 163050 163054 163060 163062 163068 163072 163074 163078 163084 163090 163092 163098 163102 163104 163110 163114 163120 163128 203614
| A. | 稀有气体不活泼是因为它们原子最外层都达到8e-稳定结构 | |
| B. | 原子序数为12的元素位于元素周期表的第三周期ⅡA族 | |
| C. | 第二周期ⅣA族元素的原子核电荷数和中子数一定为6 | |
| D. | ⅦA族元素是同周期主族元素中原子半径最大的 |




 .
. .
.