13.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温下,23g NO2含有NA 个氧原子 | |
| B. | 1 L 0.1 mol/L NaHSO3溶液中含有的HSO3-数目为0.1 NA | |
| C. | 1 L pH=1 的硫酸溶液中含有的H+ 数为0.2 NA | |
| D. | 标准状况下,2.24 L CO 和CO2混合气体中含有的氧原子数为0.15NA |
12.化学与生活密切相关,下列说法不正确的是( )
| A. | 用燃烧法可鉴别羊毛制品和涤纶制品 | |
| B. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 | |
| C. | 二氧化硫可广泛用于食品的增白 | |
| D. | 次氯酸钠溶液可用于环境的消毒杀菌 |
11.下列相关数值判断正确的是( )
| A. | 常温下,pH=2的硫酸溶液中,由水电离出的H+个数为10-12NA | |
| B. | 标准状况下,1.12L二氯甲烷含氯离子数为0.2NA | |
| C. | 向过量FeI2溶液中通入Cl2,当有1mol Fe2+被氧化时,转移的电子数为3NA | |
| D. | 2molNH3与3molO2在催化剂作用下加热充分反应后,所得NO分子数小于2NA |
10.下列离子方程式书写正确的是( )
| A. | 碳酸钙与醋酸反应:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO- | |
| B. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| C. | NaHCO3溶液显碱性:HCO3-+H2O═CO32-+H3O+ | |
| D. | 碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |
9.下列实验方案设计正确的是( )
| A. | 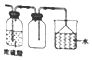 利用图收集干燥的氯化氢气体 | |
| B. | 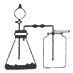 选择合适的试剂,利用图2可分别制取并收集少量CO2、NO和O2 | |
| C. |  利用图可验证铁发生吸氧腐蚀 | |
| D. |  利用图蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
8.利用如图所示的装置可将CO2转化为燃料甲醇,下列说法正确的是( )


| A. | b极发生还原反应 | |
| B. | a极的电极反应:CH3OH+H2O-6e-═CO2+6H+ | |
| C. | 总反应方程式为:2CO2+4H2O$\frac{\underline{\;通电\;}}{\;}$2CH3OH+3O2 | |
| D. | 该装置将化学能转变为电能 |
7.水杨酸、冬青油、阿司匹林都是常用西药,它们的结构简式如表:以下说法不正确的是( )
| 有机物 | 水杨酸 | 冬青油 | 阿司匹林 |
结构简式 |  |  | 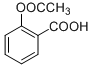 |
| A. | 可以用FeCl3溶液鉴别冬青油和阿司匹林 | |
| B. | 由水杨酸制冬青油的反应是取代反应 | |
| C. | 1mol阿司匹林最多能与3 mol NaOH反应 | |
| D. | 可以用碳酸钠溶液除去冬青油中少量的水杨酸 |
6.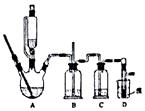 实验室制备1,2-溴乙烷的反应原理如下:
实验室制备1,2-溴乙烷的反应原理如下:
CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2+H2O CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
有关数据列表如表:
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d(填正确选项前的字母).
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)装置B的作用是安全瓶的作用.
(3)在装置c中应加入c(填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体.
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应己经结束的最简单方法是溴的颜色完全褪去.
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”).
(6)若产物中有少量未反应的Br2,最好用b(填正确选项前的字母)洗涤除去.
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(7)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
(8)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
0 162840 162848 162854 162858 162864 162866 162870 162876 162878 162884 162890 162894 162896 162900 162906 162908 162914 162918 162920 162924 162926 162930 162932 162934 162935 162936 162938 162939 162940 162942 162944 162948 162950 162954 162956 162960 162966 162968 162974 162978 162980 162984 162990 162996 162998 163004 163008 163010 163016 163020 163026 163034 203614
 实验室制备1,2-溴乙烷的反应原理如下:
实验室制备1,2-溴乙烷的反应原理如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2+H2O CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
有关数据列表如表:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度(g/cm3) | 0.79 | 2.2 | 0.71 |
| 沸点(℃) | 78.5 | 132 | 34.6 |
| 熔点(℃) | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d(填正确选项前的字母).
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)装置B的作用是安全瓶的作用.
(3)在装置c中应加入c(填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体.
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应己经结束的最简单方法是溴的颜色完全褪去.
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”).
(6)若产物中有少量未反应的Br2,最好用b(填正确选项前的字母)洗涤除去.
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(7)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
(8)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
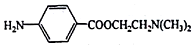 )可用作临床麻醉剂,熔点约60℃.它的一条合成路线如下图所示(部分反应试剂和条件己省略):
)可用作临床麻醉剂,熔点约60℃.它的一条合成路线如下图所示(部分反应试剂和条件己省略):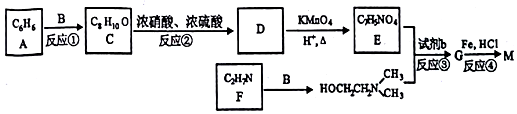
 的结构不稳定.
的结构不稳定.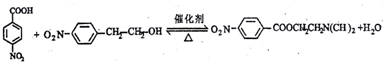 .
.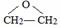 、FH3C-NH-CH3.
、FH3C-NH-CH3.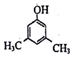 、
、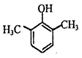 、
、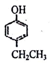 .
.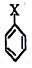 ,若-X为烃基或羟基,再次取代时,新取代基在-X的邻位或对位;若-X为羧基或硝基,再次取代时,新取代基在-X的间位.参照上述合成路线,设计由甲苯合成
,若-X为烃基或羟基,再次取代时,新取代基在-X的邻位或对位;若-X为羧基或硝基,再次取代时,新取代基在-X的间位.参照上述合成路线,设计由甲苯合成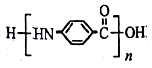 的合成路线(用合成路线流程图表示,并注明反应条件,合成过程中无机试剂可任选).
的合成路线(用合成路线流程图表示,并注明反应条件,合成过程中无机试剂可任选). .
.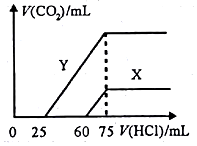 A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大.A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一.请化学用语回答下列问题:
A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大.A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一.请化学用语回答下列问题: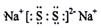 ,写出在空气中长期放置生成H的化学反应方程式为:4Na2S+O2+2H2O=4NaOH+2Na2S2.H的溶液与稀硫酸反应产生的现象为溶液由黄色变为无色,产生浅黄色沉淀和气体产生.
,写出在空气中长期放置生成H的化学反应方程式为:4Na2S+O2+2H2O=4NaOH+2Na2S2.H的溶液与稀硫酸反应产生的现象为溶液由黄色变为无色,产生浅黄色沉淀和气体产生.