题目内容
9.下列实验方案设计正确的是( )| A. | 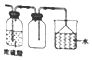 利用图收集干燥的氯化氢气体 | |
| B. | 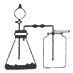 选择合适的试剂,利用图2可分别制取并收集少量CO2、NO和O2 | |
| C. |  利用图可验证铁发生吸氧腐蚀 | |
| D. |  利用图蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
分析 A.氯化氢密度大于空气,收集HCl的导管应该采用长进短出的方式;
B.NO气体与空气后者氧气反应,不能用排空气法收集;
C.铁发生吸氧腐蚀后左侧试管中压强减小,右侧导管中水面会上升;
D.氯化铵加热易分解,不能通过蒸发操作得到氯化铵晶体.
解答 解:A.HCl气体的密度比空气大,收集HCl的导管不合理,应该采用长进短出的方式,故A错误;
B.选择合适的试剂,利用图2可分别制取并收集少量CO2和O2,但NO与氧气反应,不能用排空气法收集NO气体,故B错误;
C.利用图示装置,根据右侧试管的导管中水面是否上升可验证铁发生吸氧腐蚀,故C正确;
D.氯化铵不稳定,加热易分解,蒸干NH4Cl饱和溶液无法获得NH4Cl晶体,故D错误;
故选C.
点评 本题考查化学实验方案的评价,题目难度不大,涉及气体制备与收集、金属腐蚀类型、物质制备等知识,明确常见化学实验基本操作方法即可解答,试题培养了学生的化学实验能力.

练习册系列答案
相关题目
4.乙醇转化为乙醛,发生的反应为( )
| A. | 取代反应 | B. | 加成反应 | C. | 消除反应 | D. | 氧化反应 |
20.X、Y、Z、R、W是原子序数依次增大的五种短周期元素.Y和R同主族,可组成共价化合物RY2,Y和Z最外层电子数之和与W的最外层电子数相同,25℃时,0.1mol/LX和W形成化合物的水溶液pH=1.下列说法正确的是( )
| A. | Z与Y、Z与W形成的化合物的化学键完全相同 | |
| B. | X与Y组成的简单氢化物的沸点高于X与R组成的简单氢化物的沸点,是因为非金属性Y>R | |
| C. | 简单离子的半径:Z>R>W>Y | |
| D. | Y、Z、W三种元素组成的化合物的水溶液可能显碱性 |
17.硫铁矿焙烧后的烧渣含有Fe2O3、FcO、SiO2、Al2O3,用过量硫酸浸取,过滤,将滤液分别与下列指定物质反应,所得溶液中主要存在的一组离子正确的是( )
| A. | 过量 Cl2:Fe2+、H+、Al3+、Cl-、SO42- | |
| B. | 过量SO2:Fe2+、H+、Al3+、SO42- | |
| C. | 过量氨水:NH4+、AlO2-、SO42-、OH- | |
| D. | 过量 Na2O2:Na+、Fe3+、SO42-、OH- |
14.下列叙述正确的是( )
| A. | 用硫酸清洗锅炉中的水垢 | |
| B. | Na2O2 用作呼吸面具的供氧剂 | |
| C. | 氯水中通入SO2 后溶液的酸性减弱 | |
| D. | N2 与O2 在放电条件下直接化合生成NO2 |
18.溴乙烷与NaOH乙醇溶液共热,将逸出气体通入高锰酸钾溶液.下列分析不正确的是( )
| A. | 可以观察到酸性高锰酸钾溶液褪色 | |
| B. | 溴乙烷能发生消去反应 | |
| C. | 该实验现象不能说明产生的气体中一定有乙烯 | |
| D. | 向反应后溶液中滴加AgNO3溶液可验证Br-的存在 |
11.下列说法正确的是( )
| A. | 向海水中加入净水剂明矾可使海水淡化 | |
| B. | 合成纤维、光导纤维都属于有机高分子材料 | |
| C. | 利用加热的方法杀死人体内感染的埃博拉病毒 | |
| D. | “雾”是微小水滴或冰晶组成的气溶胶系统,“霾”中的灰尘对大气中的有害物质起吸附作用 |
 A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大.A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一.请化学用语回答下列问题:
A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大.A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一.请化学用语回答下列问题: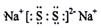 ,写出在空气中长期放置生成H的化学反应方程式为:4Na2S+O2+2H2O=4NaOH+2Na2S2.H的溶液与稀硫酸反应产生的现象为溶液由黄色变为无色,产生浅黄色沉淀和气体产生.
,写出在空气中长期放置生成H的化学反应方程式为:4Na2S+O2+2H2O=4NaOH+2Na2S2.H的溶液与稀硫酸反应产生的现象为溶液由黄色变为无色,产生浅黄色沉淀和气体产生.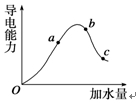 一定温度下,冰醋酸在加水稀释过程中溶液导电能力的变化曲线如图所示,请回答下列问题:
一定温度下,冰醋酸在加水稀释过程中溶液导电能力的变化曲线如图所示,请回答下列问题: