16.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使甲基橙变红色的溶液中:Na+、K+、Br-、CO32- | |
| B. | 0.1 mol/LCa(ClO)2溶液中:Fe2+、A13+、I-、SO42- | |
| C. | 0.1 mol/L Fe2(SO4)3溶液中:NH4+、Cu2+、NO3-、SO42- | |
| D. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13 mol/L的溶液中:Ca2+、NH4+、CH3COO-、HCO3- |
15.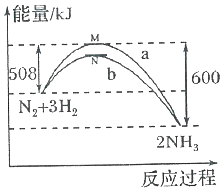 在一定温度时,N2与H2反应过程中能量变化的曲线如图,其中a表示不使用催化剂时的能量变化曲线,b表示使用催化剂时的能量变化曲线.下列叙述正确的是( )
在一定温度时,N2与H2反应过程中能量变化的曲线如图,其中a表示不使用催化剂时的能量变化曲线,b表示使用催化剂时的能量变化曲线.下列叙述正确的是( )
 在一定温度时,N2与H2反应过程中能量变化的曲线如图,其中a表示不使用催化剂时的能量变化曲线,b表示使用催化剂时的能量变化曲线.下列叙述正确的是( )
在一定温度时,N2与H2反应过程中能量变化的曲线如图,其中a表示不使用催化剂时的能量变化曲线,b表示使用催化剂时的能量变化曲线.下列叙述正确的是( )| A. | 状态M和N均表示2molN(g)+6mol H(g) | |
| B. | 该反应的热化学方程式为:N2+3H2?2NH3△H=-92kJ•mol-l | |
| C. | 使用催化剂,降低了反应进行所需的最低能量,增大了反应放出的能量 | |
| D. | 使用催化剂,并不能改变反应的△H |
14.常温下,一定浓度的某酸HA溶液的pH=5,下列有关说正确的是( )
| A. | 向溶液中加入适量NaA固体,若溶液pH不变,则HA为强酸 | |
| B. | 若HA为弱酸,则该溶液导电能力比等体积pH=5的盐酸弱得多 | |
| C. | 若HA为弱酸,则加入等体积pH=9的NaOH溶液,所得溶液pH>7 | |
| D. | 取该溶液1.00mL,加水稀释至1000mL,所得溶液pH=8 |
13.下列说法正确的是( )
| A. | H2和D2互为同位素 | |
| B. | 12C原子是指质子数为6,中子数是12的一种核素 | |
| C. | 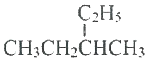 的名称是2-乙基丁烷 的名称是2-乙基丁烷 | |
| D. | 分子式为C2H6O、C4H10的有机物均有两种同分异构体 |
12.下列说法不正确的是( )
| A. | 食盐和醋可作调味剂,也可用作食品防腐剂 | |
| B. | 植物秸秆不可用来制造酒精 | |
| C. | 镁合金可用于制造火箭、导弹和飞机的部件 | |
| D. | 二氧化硅可用于制光导纤维 |
11.用下列实验装置进行相应实验,能达到实验目的是( )
| A. | 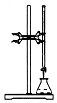 用标准氢氧化钠溶液滴定未知浓度的盐酸 | |
| B. | 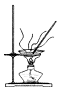 加热FeCl3溶液获取FeCl3固体 | |
| C. | 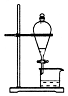 用酒精萃取碘水中的碘 | |
| D. | 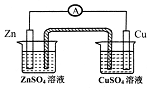 通过原电池原理证明金属性Zn>Cu |
10.化学与社会、生活密切相关.对下列化学应用的判断和解释均正确的是( )
| 选项 | 化学应用 | 判断及解释 |
| A | 燃烧法可以鉴别羊毛和棉线 | 对.羊毛的主要成分是蛋白质,燃烧有烧焦羽毛气味. |
| B | 高锰酸钾可用于水果保鲜 | 错.因为高锰酸钾会氧化水果中的有机物 |
| C | SiO2可用于制备光导纤维 | 对.因为SiO2有导电性 |
| D | 误食重金属盐引起人体中毒均可以喝大量食盐水解毒 | 对.因为食盐水有解毒功能 |
| A. | A | B. | B | C. | C | D. | D |
8.几种短周期元素的原子半径及主要化合价如表:已知X是短周期中最活泼的金属,且与R同周期.(请用化学用语答题)
(1)R的元素符号为Al; M在元素周期表中的位置为第二周期第VIA族.
(2)X与Y按原子个数比1:1构成的物质的电子式为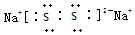 ;所含化学键类型离子键、共价键.
;所含化学键类型离子键、共价键.
(3)X+,Y2?,M2?离子半径大小顺序为S2?>O2?>Na+;.
(4)将YM2通入FeCl3溶液中的离子方程式2H2O+SO2+2Fe3+=2Fe2++SO42-+4H+.
(5)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的反应式Cu+2OH--2e-=Cu(OH)2.
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6-2 | +5-3 | -2 | +3 |
(2)X与Y按原子个数比1:1构成的物质的电子式为
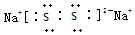 ;所含化学键类型离子键、共价键.
;所含化学键类型离子键、共价键.(3)X+,Y2?,M2?离子半径大小顺序为S2?>O2?>Na+;.
(4)将YM2通入FeCl3溶液中的离子方程式2H2O+SO2+2Fe3+=2Fe2++SO42-+4H+.
(5)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的反应式Cu+2OH--2e-=Cu(OH)2.
7. 某化学兴趣小组对铜与硝酸的反应进行下列探究.
某化学兴趣小组对铜与硝酸的反应进行下列探究.
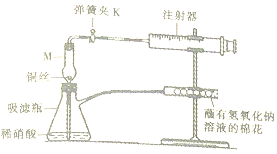
I.验证铜与稀硝酸反应生成的气体为NO如图1.
(1)仪器M的名称为干燥管
(2)完成下列表格.
Ⅱ.为验证铜与适量浓硝酸反应产生的气体中含NO,选用下列仪器(N2和O2的用量可自由控制)完成实验如图2.
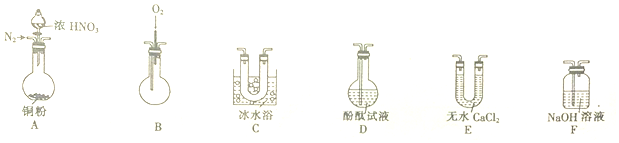
已知:
①NO+NO2+2OH-═2NO2-+H2O
②NO2、NO气体液化的温度如表.
(3)仪器的连接顺序为A→E→C→B→F.(填字母)
(4)检查装置气密性后,再加入试剂,在反应前应进行的操作是通入氮气使装置中的空气排出目的是防止NO与空气中的氧气反应生成二氧化氮.
0 162813 162821 162827 162831 162837 162839 162843 162849 162851 162857 162863 162867 162869 162873 162879 162881 162887 162891 162893 162897 162899 162903 162905 162907 162908 162909 162911 162912 162913 162915 162917 162921 162923 162927 162929 162933 162939 162941 162947 162951 162953 162957 162963 162969 162971 162977 162981 162983 162989 162993 162999 163007 203614
 某化学兴趣小组对铜与硝酸的反应进行下列探究.
某化学兴趣小组对铜与硝酸的反应进行下列探究.I.验证铜与稀硝酸反应生成的气体为NO如图1.
(1)仪器M的名称为干燥管
(2)完成下列表格.
| 操作步骤 | 实验现象 | 解释 |
| 打开弹簧夹K,拉注射器推筒,使稀硝酸吸到干燥管中并充满干燥管在关闭弹簧夹K | 仪器M中有无色气体 | 反应的化学方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O |
| 打开弹簧夹K,使干燥管中无色气体进入注射器中 | 注射器中有红棕色气体 | 反应的化学方程式为2NO+O2=NO2 |

已知:
①NO+NO2+2OH-═2NO2-+H2O
②NO2、NO气体液化的温度如表.
| 气体 | NO2 | NO |
| 液化温度 | 21℃ | -152℃ |
(4)检查装置气密性后,再加入试剂,在反应前应进行的操作是通入氮气使装置中的空气排出目的是防止NO与空气中的氧气反应生成二氧化氮.